Autores: Chumpitaz Vigil Héctor Sebastián Marcelo, Polo Luna Kevin Joaquín, Salazar Ceron Isabel Janis, Vásquez Bardales Henry Alexander, Zaña Chuquizuta Brayan Alberto
El hombre desde sus inicios buscó diferentes tipos de obtención de energía. Con el descubrimiento del fuego, los combustibles fundamentales para este caso eran la madera y el carbón. La sociedad se industrializaba cada vez más, aumentando las demandas de energía. La aparición de las máquinas de vapor originó que el carbón se use con mayor frecuencia y, con el descubrimiento de la electricidad se halló una energía inagotable que era la energía de los ríos, un recurso natural. Finalmente, el hallazgo del petróleo accedió a un desarrollo más eficaz de los motores de combustión que se aplica mayormente como un mecanismo de locomoción (Martinell Benito, Julio 1993).
En la actualidad, los seres humanos realizamos un uso de combustibles de manera directa, teniendo como primer caso la utilidad de los medios de transporte, por ejemplo los automóviles, motocicletas, aerolíneas, embarcaciones, entre otros. Además, el empleo de combustible lo observamos también en el hogar ya que es necesario para preparar nuestros alimentos, la terma que nos sirve para ducharnos, la calefacción en los ambientes de la casa, etc. Estos tipos de procesos dependen de la instalación de Centrales Termoeléctricas que permiten mediante la quema de combustibles la generación de Energía Eléctrica que se usará para diferentes finalidades.
“La combustión es un conjunto de reacciones de oxidación con desprendimiento de calor, que se producen entre dos elementos: el COMBUSTIBLE, que puede ser un sólido (Carbón, Madera, etc.), un líquido (Gasóleo, Fuel-Oil, etc.) o un gas (Natural, Propano, etc.) y el COMBURENTE, Oxígeno” (García San José, Ricardo 2001). Es decir, la combustión se da cuando le aplicamos un estímulo para que se obtenga una liberación de energía de forma violenta, luz y producción de calor. Podemos observar esta reacción inicialmente en forma de chispa y después puede llegar a transformarse en una llama dependiendo de la intensidad de la reacción. Asimismo, la reacción deja como residuo dióxido de carbono y algún otro compuesto orgánico.
Las principales propiedades de un combustible son su poder calorífico, temperatura de ignición y combustión, densidad, viscosidad, contenido de humedad y composición. Los combustibles se clasifican dependiendo de su estado en sólidos, líquidos y gaseosos.
El Petróleo
Del lat. Petroleum, aceite de roca. Es una mezcla homogénea de hidrocarburos, los cuales son una larga cadena de carbono ramificado por lo general con hidrógeno. Además, de hidrocarburos, el petróleo contiene otros compuestos orgánicos, entre los que destacan: sulfuros orgánicos, compuestos de nitrógeno y oxígeno, y trazas de compuestos metálicos (sodio, hierro, níquel, vanadio, plomo).
¿CÓMO SE FORMÓ?
Los organismos marinos animales y vegetales arrastrados por los ríos al morir se depositaron en los fondos del mar. Allí se mezclaron con las finas arenas y limos. Cuando los mares se secaron quedo una capa de sal sobre esa arcilla gredosa formada por los sedimentos de los organismos vivos. Los sedimentos se hicieron más espesos y se hundieron en el suelo marino bajo su propio peso. Millones de años después el cieno y la arena se endurecieron en esquisto y arenisca, los carbonatos precipitados y los restos de caparazones se transformaron en caliza, y los tejidos blandos de los organismos muertos pasaron a ser petróleo y gas natural.
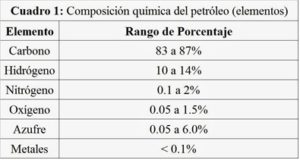
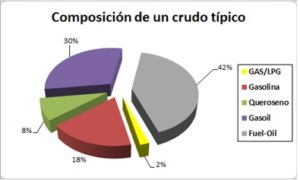
COMPOSICIÓN:
Ilustración 1: (GOB.MX 2017)
Ilustración 2: (REFINEERING 2012)
CARACTERÍSTICAS:
- Es un recurso no renovable
- A temperatura ambiente es liquido
- Es inflamable
- Es un líquido de color oscuro fluorescente con reflejos verde o verde azulado.
- Su densidad varía entre 0.615 hasta 0.994 g/cm3
- Insoluble en agua y soluble en éter, benceno, cloroformo, etc.
- Tipos de petróleo en base a su densidad: liviano, mediano, pesado y extra pesado. La densidad de relaciona con el largo de cadenas de carbono que predominan en los hidrocarburos que lo componen.
- La viscosidad varía dependiendo de su densidad.
- Posee un carácter ácido
OBTENCIÓN DEL PETRÓLEO:
- ORIGEN Y EXPLORACIÓN: Equipos móviles generan ondas sísmicas que, al rebotar sobre las diferentes capas del subsuelo, informan sobre su conformación y la presencia de petróleo
- PERFORACIÓN: Se usan equipos de rotación y sistemas de circulación de fluidos para refrigerar y para retirar los restos de petróleo.
- EXTRACCIÓN Y TRANSPORTE: El movimiento del petróleo tiene dos momentos definidos. El primero es el del traslado de la materia prima hasta la refinería. Y segundo es de los subproductos hasta los centros de consumo.
- DESTILACIÓN: El petróleo se destila en refinerías. Estas son enormes complejos donde se lo somete a procesos de separación física. Del petróleo crudo se obtienen como 8 subproductos de los que se derivan hasta otros 2000 compuestos.
Gas Natural
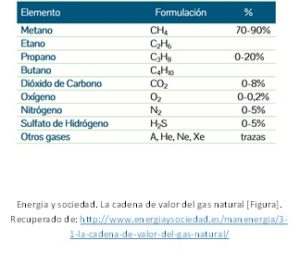 El gas natural es una mezcla de hidrocarburos que se encuentra en el subsuelo. Puede presentarse solo, en estado “libre”, o mezclado con otros hidrocarburos u otros gases del yacimiento, en estado “asociado”. Se compone principalmente por metano, siendo este un 70-90% aproximadamente del total de la mezcla.
El gas natural es una mezcla de hidrocarburos que se encuentra en el subsuelo. Puede presentarse solo, en estado “libre”, o mezclado con otros hidrocarburos u otros gases del yacimiento, en estado “asociado”. Se compone principalmente por metano, siendo este un 70-90% aproximadamente del total de la mezcla.
El gas natural se origina de la descomposición, durante miles de años, de materia orgánica enterrada con otros sedimentos en yacimientos a grandes profundidades, altas presiones y altas temperaturas; por lo que se le considera un combustible fósil. Es un gas incoloro e inodoro cuya combustión es más limpia en comparación con otros gases ya que emite menor cantidad de CO2 y contiene bajas cantidades de NO2, CO, S, entre otros.
El gas natural es una fuente importante de energía, de tipo no renovable, que se utiliza como combustible en los sectores industrial, comercial y doméstico, así como para la generación de electricidad.
EXPLORACIÓN, EXTRACCIÓN Y PRODUCCIÓN DEL GAS NATURAL
- Exploración: Para extraer el gas natural se realizan algunos estudios, pruebas, análisis geológicos necesarios para descubrir la presencia de hidrocarburos gaseosos; así como, para identificarlos y cuantificarlos.
- Extracción: Una vez que se tiene ubicado el recurso se planifica su extracción lo cual consiste en una serie de actividades que permiten extraer el gas del yacimiento y separarlo, en el caso se encuentre en estado asociado. La reserva es “aprobada” cuando se determina la cantidad y calidad del gas del yacimiento, además de la duración en relación a la cantidad y la rentabilidad del proyecto; es decir, si existe una gran demanda de este, si el precio de venta es alto, etc.
Generalmente, se utiliza una técnica de perforación por rotación directa; es decir, la materia perforada se traslada a la superficie a través del interior del brazo perforador. El desarrollo reciente de las técnicas de perforación horizontal permite acceder a yacimientos más alejados desde una misma plataforma de extracción.
- Producción: Una vez extraído el gas natural es necesario procesarlo para su transporte y comercialización, respetando los estándares de seguridad e infraestructuras en los puntos de entrega. En dicho proceso se separan aquellos gases que no aportan energía y aquellos elementos que pueden generar accidentes durante la combustión del gas natural. Finalmente se distribuye mediante el uso de los gaseoductos y tuberías que salen directamente de los tanques de almacenamiento.
El carbón
“Es una sustancia fósil, que se encuentra bajo la superficie terrestre, de origen vegetal, generada como resultado de la descomposición lenta de la materia orgánica de los bosques” (VILLALBA 2015).
“El principal componente del carbón mineral es carbono (entre un 75 a un 90 %) y algunos hidrocarburos. Aunque su uso directo es muy contaminante, actualmente se busca desarrollar tecnologías para lograr una combustión más limpia y respetuosa del medio ambiente. Pese a esto, el uso del carbón como energético es muy alto, ya que corresponde a cerca de la cuarta parte de la energía consumida de manera directa en todo el mundo” (MINEDUC 2012).
El análisis elemental es un ensayo químico que proporciona la fracción másica, modo de expresar la concentración de una disolución (la cantidad de soluto que contiene), de cada uno de los cinco elementos que componen principalmente todos los tipos de carbón: carbono (C), nitrógeno (N), oxígeno (O), hidrógeno (H), azufre (S).
Procesos de formación
- El carbón se origina a partir de la densa vegetación que crece en lugares pantanosos. Poco se conoce acerca de las reacciones químicas que se encuentran involucradas en este proceso.
- La energía que se dispone a partir de la combustión del carbón fue almacenada durante el proceso de fotosíntesis en el vegetal.
- El tiempo y la temperatura son probablemente bastante importantes en la determinación del contenido de carbono del carbón, el cual nunca se encuentra libre.
Carbonificación
La carbonificación comprende los procesos que transforman los restos vegetales en carbón, que cuanto mayor sea esta transformación, mayor será el grado de carbonificación o rango del mismo.
- Carbonificación bioquímica:
Se comprenden aquí todas las transformaciones como consecuencia de la acción de hongos y bacterias aeróbicas en una primera etapa y en una segunda etapa, bacterias anaeróbicas. El resultado es el paso de turba a lignito.
- Carbonificación geoquímica:
Consiste en los procesos físico-químicos de transformación sufridos durante el enterramiento de la materia orgánica, donde los principales agentes transformadores son la presión (litostática y tectónica favorecen, hidrostática desfavorece), la temperatura (a mayor temperatura más rango) y el tiempo (a igualdad de otros factores más tiempo, implica más rango).
El resultado es el aumento en el poder calorífico y concentración de C, así como la pérdida de O, H, H2O y materias volátiles, aumento de la compactación, dureza, densidad y reflectancia. El rango del carbón pasa de:
Madera → turba → lignito → hulla → antracita → metantracita → grafito.
Clasificación del carbón
A medida que pasaba el tiempo, el carbón aumentaba su contenido en carbono, lo cual incrementa la calidad y poder calorífico del mismo.
Según este criterio duración y condiciones (presión y temperatura) del proceso de carbonización, el carbón se puede clasificar en los siguientes tipos:
- Turba: Tiene un porcentaje alto de humedad, bajo poder calorífico y poco carbono.
- Lignito: Mayor poder calorífico, mayor contenido en carbono y mucha humedad. Se encuentra en minas a cielo abierto y por eso, su uso suele ser rentable.
- Hulla: Alto poder calorífico y elevado porcentaje de carbono. Carbón duro, totalmente carbonizado. Color negro lustroso.
- Antracita: Es el carbón más antiguo, pues tiene más de un 90% de carbono, duro y totalmente carbonizado.
La presión y el calor adicional pueden transformar el carbón en grafito (estructura interna diferente a la del carbono).
A través de una serie de procesos, se obtienen los carbones artificiales; los más importantes son el coque y el carbón vegetal.
- Coque: Es una sustancia carbonosa, sólida, ligera, negra y lustrosa que se obtiene a partir del carbón. El resultado es un carbón con un mayor poder calorífico, además de una serie de productos volátiles (gas ciudad, amoníaco, alquitrán).
- Carbón vegetal: se obtiene por destilación seca de la madera. Puede usarse como combustible, pero su principal aplicación es como absorbente de gases.
Los reactivos para la producción de gas son el carbón, oxígeno y vapor:
2 C + O2→2 CO combustión; ∆H = – 214 kJ
2 CO + O2→2 CO2 combustión; ∆H = – 561 kJ
C + H2O→CO + H2 gasificación; ∆H = 131 kJ
CO + H2O→CO2+ H2 reacción con vapor de agua; ∆H = 29 kJ
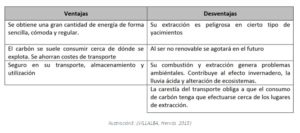
Ventajas y desventajas del carbón
Aplicaciones
Poder Calorífico de los combustibles
También llamada potencia calorífica; La potencia calorífica de un combustible es la energía liberada por unidad de peso o de volumen de este. Puede determinarse por cálculo o mediante el empleo de un calorímetro y se realiza quemando una pequeña parte del combustible en una bomba calorimétrica. El calor desprendido se cede a una masa de agua en un sistema adiabático. Este calor se determina por el aumento de temperatura del agua.
Ahora veremos algunos valores de poder calorífico de los principales combustibles:
Carbón:
El contenido principal de este sólido es carbono, que va desde una concentración de 50% en la turba, hasta un 90% en la hulla y tiene un poder calorífico de aproximadamente 7000 kcal/kg (2), cantidad que aumenta o disminuye según el contenido de carbono.
Dentro de los diferentes tipos de carbones se tiene:
| PCI (GJ/t) |
PCI (kWh/Kg) |
PCI (kcal/Kg) |
PCI (tep/t) |
|
| Antracita eléctrica | 19.23 | 5.34 | 4,594 | 0.4594 |
| Antracita industrial | 24.40 | 6.78 | 5,829 | 0.5829 |
| Antracita otros sectores de consumo final | 26.10 | 7.25 | 6,235 | 0.6235 |
| Hulla eléctrica | 22.60 | 6.28 | 5,399 | 0.5399 |
| Hulla coquizable | 29.55 | 8.21 | 7,059 | 0.7059 |
| Hulla altos hornos | 26.20 | 7.28 | 6,259 | 0.6259 |
| Hulla industrial | 24.10 | 6.69 | 5,757 | 0.5757 |
| Hulla otros sectores de consumo final | 26.86 | 7.46 | 6,417 | 0.6417 |
| Carbón subbituminoso | 13.37 | 3.71 | 3,194 | 0.3194 |
| Lignito | 13.34 | 3.71 | 3,195 | 0.3195 |
| Coque de coquería | 26.80 | 3.71 | 3,195 | 0.3195 |
| Alquitrán de hulla | 38.00 | 3.71 | 3,195 | 0.3195 |
Ilustración 5: (Eurosta 2013)
Petróleo:
Combustible natural líquido formado por una mezcla de hidrocarburos y obtenido de la transformación de plancton, por acción de bacterias y tiene ventaja en poder calorífico con respecto al carbón, con un valor que ronda las 10000 kcal/kg (Corinto 2011).
Aunque se pueden obtener distintos valores de acuerdo con sus tipos y derivados:
| PCI (GJ/t) |
PCI (kWh/Kg) |
PCI (kcal/Kg) |
PCI (tep/t) |
|
| Petróleo Bruto | 42.55 | 11.82 | 10,190 | 1.0190 |
| Materias primas de refinería | 39.88 | 11.08 | 9,550 | 0.9550 |
| GLP | 45.89 | 12.75 | 10,990 | 1.0990 |
| Propano | 46.20 | 12.83 | 11,063 | 1.1063 |
| Butano | 44.78 | 12.44 | 10,723 | 1.0723 |
| Queroseno | 42.89 | 11.91 | 10,270 | 1.0270 |
| Gasolina | 43.89 | 12.19 | 10,510 | 1.0510 |
| Gasolina aviación | 43.89 | 12.19 | 10,510 | 1.0510 |
| Gasóleo automoción | 42.47 | 11.80 | 10,170 | 1.0170 |
| Otros gasóleos | 42.47 | 11.80 | 10,170 | 1.0170 |
| Fuelóleo | 39.88 | 11.08 | 9,550 | 0.9550 |
| Alquitrán | 39.88 | 11.08 | 9,550 | 0.9550 |
| Nafta | 43.89 | 12.19 | 10,510 | 1.0510 |
| Lubricantes | 39.88 | 11.08 | 9,550 | 0.9550 |
| Coque de petróleo | 31.90 | 8.86 | 7,640 | 0.7640 |
Ilustración 6: (Eurosta 2013)
Gas natural:
El gas natural está formado principalmente por metano, aunque puede contener pequeñas cantidades de otros compuestos como el etano y dado que contiene poca cantidad de otros compuestos, tiene una combustión más limpia con un poder calorífico que ronda las 1000 kcal/m3 (Corinto 2011).
Valores de poder calorífico de sus compuestos y similares (gas de refinería):
| PCI (GJ/t) |
PCI (kWh/Kg) |
PCI (kcal/Kg) |
PCI (tep/t) |
|
| GNL | 45.10 | 12.53 | 10,800 | 1.0800 |
| Metano | 50.00 | 13.89 | 11,973 | 1.1973 |
| Etano | 47.51 | 13.20 | 11,350 | 1.1350 |
| Gas de refinería | 49.36 | 13.71 | 11,820 | 1.1820 |
Ilustración 7: (Eurosta 2013)
BIBLIOGRAFÍA
- BLOG DEL PETRÓLEO
2017 Blog del petróleo: conceptos fundamentales. Consulta: 01 de marzo del 2018
http://blogdelpetroleo.blogspot.pe/
- CORINTO
2011 Química General. Consulta: 02 de marzo de 2018.
http://corinto.pucp.edu.pe/quimicageneral/contenido/51-principales-fuentes-de-energia-quimica.html
- ECOPETROL
2017 ¿Qué es el gas natural? Consulta: 02 de marzo de 2018
https://www.ecopetrol.com.co/wps/portal/es/ecopetrol-web/productos-y-servicios/productos/gas-natural/Informaci%C3%B3n%20General/que-es-el-gas-natural/!ut/p/z0/04_Sj9CPykssy0xPLMnMz0vMAfIjo8ziLQIMHd09DQy9DZwt3QwcjTwsQxw9g4I8nIz0C7IdFQEONbdQ/
- ENERGÍA Y SOCIEDAD
2016 La cadena de valor del gas natural. Consulta: 02 de marzo de 2018.
- ESPAÑA, Universidad de Córdoba
2016 “Combustibles fósiles e hidrógeno”. España. Consulta 28 de marzo de 2018.
http://www.uco.es/~iq2sagrl/Fuentes%20energia/TranspTema2.pdf
- ESPAÑA, Universidad de Oviedo
2016 “Combustibles industriales”. España. Consulta 29 de marzo de 2018.
http://www6.uniovi.es/usr/fblanco/CombustiblesINDUSTRIALES.2006.pdf
- GAMALLO GARCÍA Martín, FERNANDEZ Martín y CAÑOTO Aida
2011 La importancia de la química del carbono. Consulta 2 de abril de 2018.
- GARCÍA SAN JOSÉ, Ricardo
2001 Combustión y Combustible. Consulta: 29 de marzo de 2018
file:///C:/Users/hecto/Downloads/Combusti%C3%B3n%20y%20combustibles%20(1).pdf
- GOBIERNO DE CHILE, Ministerio de Educación
2012 “La materia orgánica y los combustibles fósiles”. Materia y entorno. Chile. Consulta 30 de marzo de 2018
http://epja.mineduc.cl/wp-content/uploads/sites/43/2016/04/la_materia_organica_y_los_combustibles_fosiles.pdf
- MX 2017 Características del petróleo. Consulta: 01 de marzo del 2018
https://www.sgm.gob.mx/Web/MuseoVirtual/Aplicaciones_geologicas/Caracteristicas-del-petroleo.html
- LA GUÍA DE LA QUÍMICA
2016 Reservas, extracción y producción. Consulta: 02 de marzo de 2018.
- LA GUÍA DE LA QUÍMICA
2017 Gas natural. Consulta: 02 de marzo de 2018.
- LATAMISRAEL
2017 Catalizadores químicos para convertir gas natural en combustible líquido. Consulta 1 de abril de 2018
Catalizadores químicos para convertir gas natural en combustible líquido.
- MARTINELL BENITO, Julio
1993 Los prometeos modernos o el esfuerzo para controlar la fusión nuclear. Dos volúmenes. México: FONDO DE CULTURA ECONÓMICA (FCE). Consulta: 29 de marzo de 2018.
http://bibliotecadigital.ilce.edu.mx/sites/ciencia/volumen2/ciencia3/106/htm/sec_3.htm
- MÉXICO, Universidad autónoma del Carmen facultad de química
2015 Gas natural. Consulta 1 de abril de 2018
http://quieroapuntes.com/gas-natural_endulzamiento.html
- MOSCOSO PANTOJA, Marcelo
2017 Los combustibles convencionales sobre los alternativos. Consulta 1 de abril de 2018.
https://www.natura-medioambiental.com/combustibles-convencionales-sobre-los-alternativos/
- ORTIZ, Claudia
2016 “El Petróleo”. Consulta: 01 de marzo del 2018
https://es.scribd.com/document/256812428/Quimica-Organica-El-Petroleo
- PERUPETRO
2010 Conceptos básicos sobre el gas natural [diapositiva]. Consulta: 02 de marzo de 2018.
https://www.perupetro.com.pe/wps/wcm/connect/984b352d-2ac3-4f97-815c104617f8528f/Charla+Basica+sobre+GasNatural.pdf?MOD=AJPERES
- REFINEERING
2012 “EL Petróleo”. Industria, Petroquímica. Consulta 30 de marzo de 2018.
- RIVERA, Norma
2012 “Fracción másica y fracción molar”. Universidad Politécnica de Valencia. Consulta 30 de marzo de 2018.
https://es.slideshare.net/nriverapazos/fraccin-msica-y-fraccin-molar-definiciones-y-conversin
- VILLALBA, Hervás
2015 “Combustibles fósiles”. Tecnología Industrial. Consulta 29 de marzo de 2018.
https://iesvillalbahervastecnologia.files.wordpress.com/2013/10/combustibles-fosiles.pdf
- Eurosta, AIE y Resolución de la Secretaría de Estado de Energía de 27 de diciembre de 2013 que modifica a la Orden ITC/2877/2008.
Fuentes de las imágenes
Mendez Fernandez, Jesus Gilberto. Universidad Autónoma Del Carmen. Consulta: 30 de marzo de 2018. http://biblioteca.unmsm.edu.pe/redlieds/proyecto/publicacioneselectro/monografias/OPTIMIZACION%20DEL%20%20PROCESO%20DE%20ENDULZAMIENTO%20DEL%20GAS%20NATURAL.pdf
LatamIsrael. (2017). Catalizadores químicos para convertir gas natural en combustible líquido. Consulta: 30 de marzo de 2018. https://latamisrael.com/gas-natural/
Gamallo García, Martín y otros. (2011). La importancia de la química del carbono. Consulta: 29 de marzo de 2018. https://es.slideshare.net/descubrirlaquimica/la-importancia-de-la-qumica-del-carbono
Requena, Alejandro. (2012). Estructuras químicas del carbón. Consulta: 30 de marzo de 2018. https://es.slideshare.net/alejandrorequena/estrucutras-qumicas-en-el-carbn-12296371
Ramirez, Katheleen. (2013). El carbón y sus consecuencias como fuente de energía. Consulta: 31 de marzo de 2018. http://massielrp.blogspot.pe/