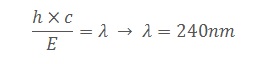*La imagen fue diseñada por uno de los integrantes del grupo OLIMPIKUS
La atmósfera está seccionada de acuerdo a las composiciones y grados de temperatura presentes en los diferentes rangos de distancia. Una de esas capas es la estratosfera (40km de espesor) donde se halla en abundancia compuestos de oxígeno como el O2, O3 y el O además de nitrógeno. Esta región atmosférica cambia su temperatura respecto de su altitud, debiéndose a que el oxígeno es muy reactivo y puede reaccionar entre sí en diversas situaciones exotérmicas dentro de un ciclo definido gracias a la energía proporcionada por la radiación UV. De esta manera se forma el ozono, el cual también se descompone y no permite que los rayos UV lleguen a la superficie. La primera de estas reacciones es la fotodisociación del oxígeno molecular, que tiene energía de enlace de 498,7kJ/mol. Entonces se tiene:
donde se encuentra el valor máximo de longitud de onda para que se suscite la reacción. Luego, se formula lo siguiente:
O2 → O + O
Sin embargo, aún existen oxígenos moleculares libres que pueden reaccionar con el producto anterior para formar el ozono (O3) según:
O + O2 + M → O3 + M
donde M es inerte y no reacciona con el oxígeno, únicamente absorbe el exceso de calor liberado con el fin de que el ozono no se descomponga espontáneamente. En consecuencia, el ozono (O3) ahora es capaz de convertirse en O y O2 gracias a la aparición de nuevos rayos ultravioleta (luz UV) de longitudes de entre 200 y 300nm:
O3 → O + O2
Así, la capa de ozono evita a través de un ciclo de reacciones químicas exotérmicas que los rayos UV atraviesen la estratosfera hasta llegar a la superficie terrestre donde su presencia puede resultar nociva.
Aspectos de la actividad humana que más influyen en la generación del problema
La comunidad científica comenzó a alarmarse por los daños ocasionados por diferentes compuestos químicos utilizados por nosotros. Algunos de ellos son los siguientes:
- Uso del CFC (clorofluorocarburos), aerosoles y sustancias que desestabilizan la molécula de ozono (O3): Así como se crean las moléculas de ozono, su contacto con ciertos componentes químicos puede desintegrarlas. Uno de ellos es el CFC. En las últimas décadas del siglo pasado existió una masiva producción de numerosos productos que contenían CFC. Este era liberado en grandes cantidades a la atmósfera y al llegar a la capa de ozono, afectado también por la radiación ultravioleta, se desintegraban en átomos individuales. El átomo de cloro liberado del CFC reaccionaba con el ozono y producía moléculas de monóxido de cloro y oxígeno, destruyendo así el ozono.
- Uso de otros refrigerantes gaseosos
Asimismo, algunas de las consecuencias que se han asociado al adelgazamiento de la capa de ozono han sido las siguientes a mencionar:
- Paso libre de las ondas ultravioleta: Una gran parte de la radiación ultravioleta, en especial la radiación uv-b, es dañina para los organismos vivos en la tierra. La capa de ozono funciona en la estratosfera como un escudo que protege a los organismos y ecosistemas de los efectos malignos de una parte de la radiación ultravioleta.
- Proliferación del cáncer en la piel (debido a los rayos UV): Asimismo, en los seres humanos, la radiación ultravioleta estimula la formación de vitamina D, pero en exceso puede aumentar el ritmo de las mutaciones en el cuerpo de los seres vivos y, por lo tanto, incrementar las probabilidades de que ocurran mutaciones malignas, como, por ejemplo, melanoma o cáncer de piel.
- Incremento de la temperatura en los casquetes polares y desalinización del mar a causa del deshielo en los polos geográficos: Cada año ocurre una disminución de hasta el 70% de la cobertura de la capa de ozono sobre la Antártida, lo que expone al planeta entero a un flujo constante de radiación.
Relación del adelgazamiento de la capa de ozono con los combustibles fósiles:
Si bien el adelgazamiento de la capa de ozono está estrechamente relacionado con los clorofluocarbonos (CFC) principalmente provenientes de los aerosoles, también existe relación de este problema ambiental a causa de los combustibles fósiles. La combustión de estos genera los llamados óxidos nitrogenados, un claro ejemplo es cuando son liberados a través del tubo de escape de vehículos, entre estos se tiene la combustión del carbón, petróleo o gas. Estos óxidos nitrogenados se combinan con derivados del cloro y del bromo lo que causa modificaciones en el frágil equilibrio de la capa de ozono. Esto es debido a que al llegar a la estratosfera se descompone mediante reacciones fotoquímicas lo cual causa la destrucción de la capa de ozono.
Referencia bibliográfica:
CHANG, RAYMOND Y KENNETH GOLDSBY
2013 Química. Undécima edición. Madrid: McGraw-Hill-Interamericana. Consulta: 28 de octubre del 2016.
PONCE, FRANCISCO
2015 “Día internacional preservación sobre la capa de ozono” [caricatura]. Consulta: 4 de noviembre de 2016.
http://franciscoponce.com/archives/34405
Guillermo M.; Miguel H.; Edgar R.; Gómez E. Capa de ozono: destrucción de la capa de ozono. Recuperado el 4 de noviembre del 2016, de: http://www.pla.net.py/enlaces/cnelm/980617/capozon.htm
Tema 10: Contaminación de la atmosfera. Sustancias que contaminan la atmosfera. Recuperado el 4 de noviembre del 2016, de: http://www4.tecnun.es/asignaturas/Ecologia/Hipertexto/10CAtm1/200Conta.htm
Imagen portada. As the pendulum swings. Spitting Fire. Recuperado el 4 de noviembre del 2016, de: https://asthependulumswings.wordpress.com/2011/09/01/spitting-fire/
Imagen portada. This date in science: Sweden goes first to ban aerosol sprays. Recuperado el 4 de noviembre del 2016, de : http://en.es-static.us/upl/2014/01/aerosol_spray-300×214.jpg
Imagen portada. Imágenes 4 ever: Sol detrás de la tierra. Recuperado el 4 de noviembre del 2016, de: http://imagenes.4ever.eu/naturaleza/universo/sol-detras-de-la-tierra-182934