Autores:
-
Bolo Lívano, Loribeth Maricielo
-
Sanchez Cueva, Araceli
-
Ramos Lazo, Ariana Massiel
-
Vergara Lezama, Joaquín Rodrigo
Introducción
Los metales y minerales desempeñan un papel importante en el desarrollo de la sociedad. Pues tecnologías como celulares, carros electrónicos o paneles solares son producidas a partir de la extracción de estos. También promueven el crecimiento económico, por ejemplo, el Perú, a nivel mundial, es uno de los principales productores de plata, zinc, cobre, plomo, oro; y las exportaciones mineras representan aproximadamente el 60% de las exportaciones del país.
En el 2018, se anunció el descubrimiento de la mina de “oro blanco” más grande del mundo, el yacimiento de Falchani. Se descubrió alrededor de 2,5 millones de toneladas de litio y una gran cantidad de uranio, que tienen en promedio una ley de 3 500 a 4 000 ppm, siete veces la cantidad de otras salares importantes, lo cual demuestra que es un potencial económico enorme. Sin embargo, esta noticia ha generado una preocupación por parte de la población local y regional con respecto al impacto de este proyecto. Entonces, ¿cuáles son las ventajas y desventajas de la explotación de la mina de litio descubierta en Perú?, ¿el impacto es en su mayoría positivo o negativo? Antes de abordar estas preguntas, se desarrollarán algunas definiciones para tener una mejor comprensión del tema.
¿Qué es un mineral?
En la actualidad, existen 5.514 minerales en el planeta, reconocidos por la Asociación Mineralógica Internacional (IMA). En rasgos generales “un mineral es un elemento o compuesto químico que normalmente es cristalino y que se ha formado como resultado de procesos geológicos” (Nickel, 1995, p. 689). Tomando en cuenta la definición geológica, son sustancias sólidas inorgánicas que aparecen de forma natural en la corteza terrestre, de composición química definida y estructura cristalina.
Video 1: ¿QUÉ ES UN MINERAL?
- Significado de ley de un mineral y pureza
La ley de un mineral se refiere a la concentración del mineral extraído presente en las rocas y en el material mineralizado de un yacimiento. Sirve para determinar la rentabilidad de la extracción de un elemento dentro de una mena. Del mismo modo, hace referencia al grado de pureza. Los minerales suelen encontrarse con cierto grado de impureza por lo que llamamos pureza de una sustancia a la relación entre masa obtenida del elemento compuesto con la masa total del compuesto.
Fórmula de composición porcentual. Fuente: http://blog.pucp.edu.pe/blog/qm2-202-131/2019/06/15/metales-y-minerales-2/
- Composición porcentual
Conocida la composición porcentual de un compuesto o su composición elemental en gramos, nos permite conocer la cantidad del elemento que queremos extraer del mineral. Y para ello se aplica la siguiente fórmula:
Fórmula de composición porcentual. Fuente: http://blog.pucp.edu.pe/blog/qm2-202-131/2019/06/15/metales-y-minerales-2/
n: número de moles del metal por cada mol de mineral.
Por ejemplo: Por ejemplo, calcular la composición porcentual en masa de hierro (Fe), en 4 moles de magnetita (Fe3O4) recurriremos a la fórmula:
Ejemplo de fórmula de composición porcentual. Fuente: http://blog.pucp.edu.pe/blog/qm2-202-131/2019/06/15/metales-y-minerales-2/
¿Qué son los metales?
Se consideran metales a los que tienen como característica ser buenos conductores de calor y electricidad. En la tabla periódica son los más numerosos y tienen altas densidades, la mayoría son sólidos a temperatura ambiente, a excepción del mercurio. Los metales han sido desde el origen de los tiempos la base de nuestra civilización, estando presentes en nuestras herramientas y enseres domésticos, en nuestras viviendas y medios de transporte, e incluso en nuestros símbolos de poder, ya sea en las joyas que nos adornan o en las armas con las que nos defendemos (Ondarse, 2021).
La importancia que los metales tienen y han tenido a lo largo de la historia es que han servido a la humanidad desde tiempos remotos gracias a sus particulares propiedades físicas intrínsecas que lo vuelven un material idóneo para formar herramientas, estatuas y estructuras de todo tipo. En este ensayo se presenta una breve descripción del mundo de los metales, sus principales características y aplicaciones, las formas que tenemos de obtenerlos y los procesos industriales que son necesarios para su transformación. De esta manera se pretende dar a conocer las diferentes vertientes de nuestra industria primaria y concienciar a los lectores de la indudable necesidad de esta actividad para mantener nuestro estilo de vida, pero dentro de los parámetros de la sostenibilidad medioambiental (Junta de Castilla y León, 2008).

Metales. Fuente: http://1.bp.blogspot.com/-9CdVEHXcqqg/UyCpY_WThVI/AAAAAAAAAH8/bbcxRC9CV4g/s1600/cobre_metales.jpeg
Desde la perspectiva física presentan gran dureza y tenacidad, un intenso y característico brillo, unas excelentes propiedades mecánicas tales como la ductilidad, maleabilidad, etc.) y una gran capacidad como conductores del calor y de la corriente eléctrica. Estas características determinan una larga vida útil, gran resistencia y fácil manipulación y transformación. La dureza y tenacidad de los metales permite su uso en piezas mecánicas sometidas a desgaste (engranajes, cojinetes, bulones, etc.); el brillo ha permitido su empleo como elemento decorativo, como base de espejos o en distintos elementos ópticos; la alta ductilidad permite la elaboración de hilos o alambres de hasta unas pocas centésimas de milímetro; mientras que la alta maleabilidad permite su transformación en chapas o láminas. Su gran capacidad para conducir el calor permite su empleo, por ejemplo, en intercambiadores térmicos, mientras que la baja resistividad eléctrica permite todas las aplicaciones eléctricas y electrónicas tales como cableados y soldaduras (Junta de Castilla y León, 2008)
Según Castilla y León (2008), los metales aparecen normalmente en estado sólido a temperatura ambiente, excepto el mercurio que es líquido, y sus puntos de fusión son muy variables, desde unos pocos grados por encima de la temperatura ambiente, como el galio a 29,8 ºC, hasta valores que alcanzan los 3.410 ºC como el caso del wolframio, lo que le convierte en prácticamente refractario e infusible. Estas propiedades son de gran utilidad en la industria, por ello el mercurio se emplea por ejemplo en interruptores de movimiento y el wolframio constituye los filamentos de las bombillas, que alcanzan la incandescencia sin llegar a fundirse. Los puntos de ebullición son igualmente muy variables desde 357 ºC para el caso del mercurio, hasta 5.930 ºC en el caso del wolframio. Otra propiedad interesante de los metales es su elevada densidad, con valores que llegan a alcanzar los 22,6 g/cm3 en el caso del osmio. Esta diferencia de densidades entre los distintos metales permite aplicaciones industriales especiales, como la sustitución de elementos de acero, que tiene una densidad de unos 7,8 g/cm3, por otros de aluminio cuya densidad es sensiblemente menor (2,7 g/cm3), por ejemplo, en las carrocerías de los automóviles.
A continuación, se presenta los tipos de metales que existen:
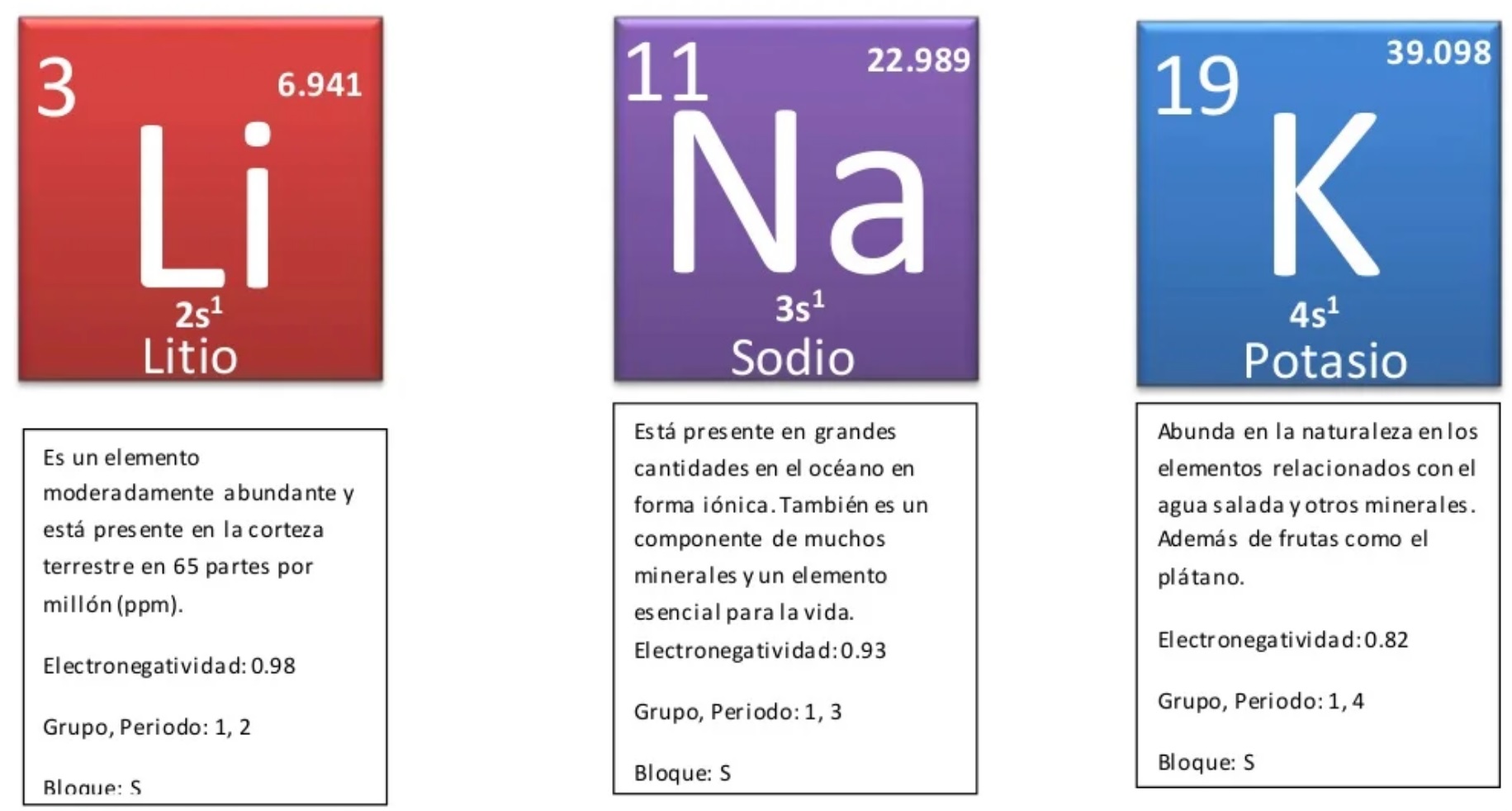
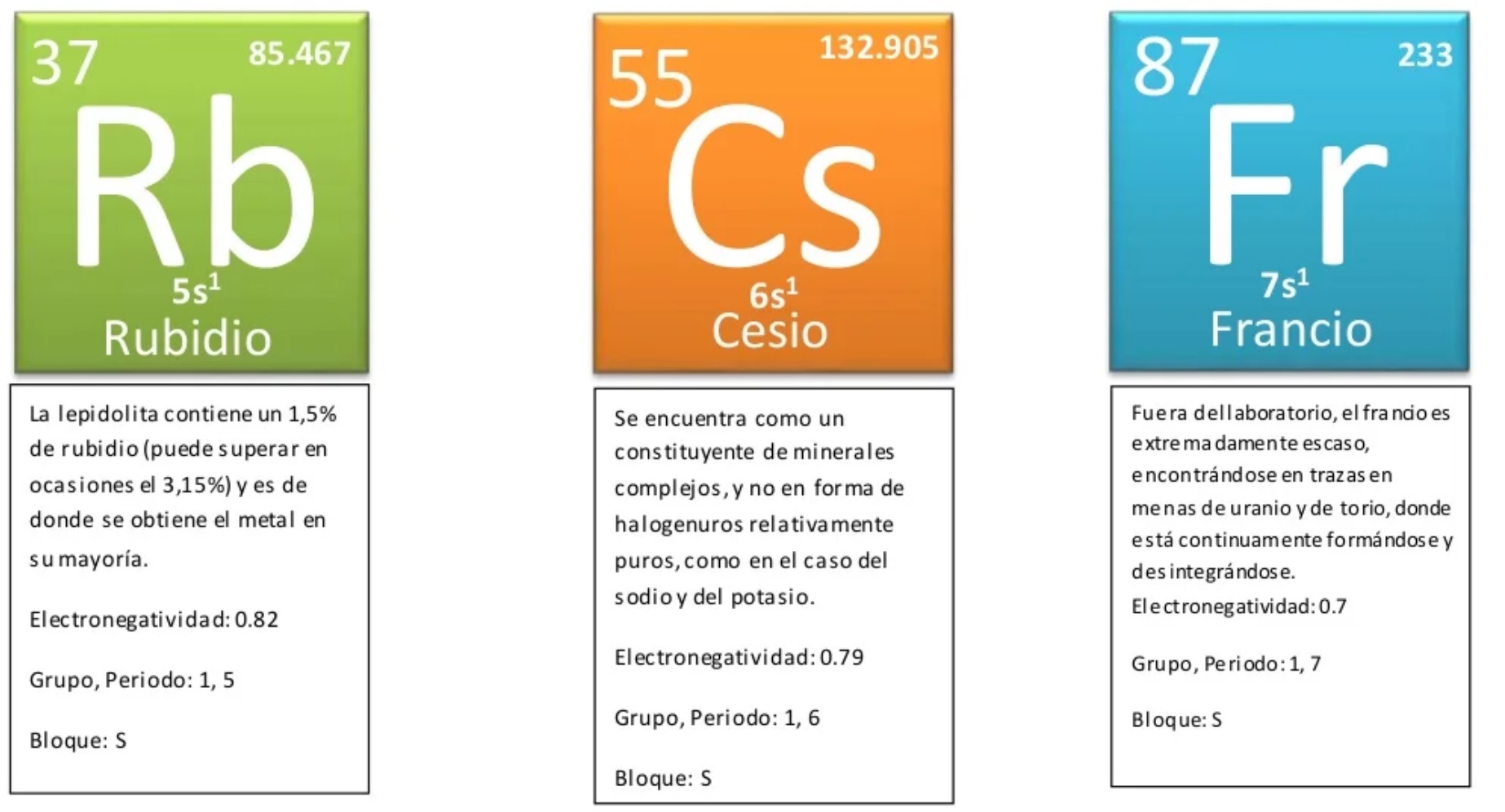
- Metales alcalinos
Son brillantes, blandos y muy reactivos a condiciones normales de presión y temperatura (1 atm y 25º C), por lo que nunca están puros en la naturaleza. Además, tienen bajas densidades y son buenos conductores del calor y la electricidad. También tienen bajos puntos de fusión y ebullición. En la Tabla Periódica ocupan el grupo I. En este grupo además se encuentra el hidrógeno (que no es un metal).
Ejemplos: Litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs), francio (Fr).
- Metales alcalinotérreos
Están situados en el grupo II de la Tabla Periódica. Su nombre proviene de las propiedades alcalinas de sus óxidos (llamados “tierras” antiguamente). Suelen ser más duros y menos reactivos que los alcalinos. Son brillantes y buenos conductores del calor y la electricidad. Tienen baja densidad y color.
Ejemplos: Berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra).
- Metales de transición
La mayoría de los metales pertenecen a esa categoría. Ocupan la región central de la Tabla Periódica y casi todos son duros, con elevados puntos de fusión y ebullición, y buena conducción del calor y la electricidad.
Ejemplos: Escandio (Sc), titanio (Ti), vanadio (V), cromo (Cr), manganeso (Mn), hierro (Fe), cobalto (Co), niquel (Ni), cobre (Cu), zinc (Zn), itrio (Y), circonio (Zr), niobio (Nb), molibdeno (Mo), tecnecio (Tc), rutenio (Ru), rodio (Rh), paladio (Pd), plata (Ag), cadmio (Cd), lutecio (Lu), hafnio (Hf), tántalo (Ta), wolframio (W), renio (Re), osmio (Os), iridio (Ir), platino (Pd), oro (Au), mercurio (Hg), lawrencio (Lr), rutherfordio (Rf), dubnio (Db), seaborgio (Sg), bohrio (Bh), hasio (Hs), meitnerio (Mt), darmstadio (Ds), roentgenio (Rg), copernicio (Cn).
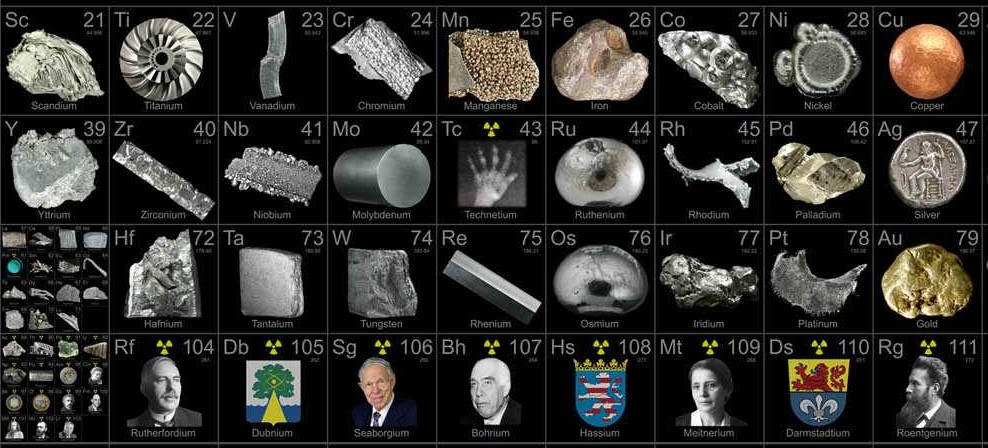
Metales de transición. Fuente: https://blog.uclm.es/fernandocarrillo/2014/10/29/los-metales-de-transicion/
- Lantánidos
También llamados lantánidos, son las llamadas “tierras raras” de la Tabla Periódica, que con los actínidos forman los “elementos de transición interna”. Son elementos muy similares entre sí, y a pesar de su nombre, son muy abundantes en la superficie terrestre. Tienen comportamientos magnéticos (cuando interactúan con un campo magnético, por ejemplo, el campo magnético que genera un imán) y espectrales (cuando la radiación incide sobre ellos) muy característicos.
Ejemplos: Lantano (La), cerio (Ce), praseodimio (Pr), neodimio (Nd), prometio (Pm), samario (Sm), europio (Eu), gadolinio (Gd), terbio (Tb), disprosio (Dy), holmio (Ho), erbio (Er), tulio (Tm), Iterbio (Yb), lutecio (Lu).
- Actínidos
Junto a las tierras raras, forman los “elementos de transición interna”, y son muy similares entre sí. Presentan altos números atómicos y muchos de ellos son radiactivos en todos sus isótopos, lo que hace que sean sumamente escasos en la naturaleza.
Ejemplos: Actinio (Ac), torio (Th), protactinio (Pa), uranio (U), neptunio (Np), plutonio (Pu), americio (Am), curio (Cm), berkelio (Bk), californio (Cf), einstenio (Es), fermio (Fm), mendelevio (Md), nobelio (No), lawrencio (Lr).
- Transactínidos
También llamados “elementos superpesados”, son aquellos que superan en número atómico al más pesado de los actínidos, el lawrencio (103).
Ejemplos: Rutherfordio (Rf), dubnio (Db), seaborgio (Sg), bohrio (Bh), hassio (Hs), meitnerio (Mt), darmstadio (Ds), roentgenio (Rg), copernicio (Cn), nihonio (Nh), flerovio (Fl), moscovio (Mc), livermorio (Lv), teneso (Ts).
¿Qué es un refinamiento?
En la producción y refinamiento de metales, una serie de reacciones físico-químicas distintas separan los componentes valiosos de las materias residuales o inservibles. El producto final es un metal que contiene cantidades mínimas de impurezas. La fundición y afino primarios producen metales directamente a partir de concentrados de minerales, mientras que la fundición y afino secundarios los producen a partir de chatarra que está formada por fragmentos y piezas de componentes metálicos, barras, virutas de torno, chapas y alambre que están fuera de especificación o desgastados, pero que puedan reciclarse y a partir de residuos de procesos (McCann, 2012).
- Tipos de refinamiento
Para producir metales refinados se utilizan generalmente dos tecnologías de recuperación, los procesos pirometalúrgicos y los hidrometalúrgicos. En los procesos pirometalúrgicos se utiliza calor para separar los metales deseados de otros materiales. En estos procesos se aprovechan las diferencias entre potenciales de oxidación, puntos de fusión, presiones de vapor, densidad y/o miscibilidad de los componentes del mineral cuando se funden. Las tecnologías hidrometalúrgicas se diferencian de los procesos pirometalúrgicos en que los metales deseados se separan de otros materiales utilizando técnicas que aprovechan las diferencias de solubilidad y/o entre las propiedades electroquímicas de los constituyentes cuando se encuentran en solución acuosa (McCann, 2012).
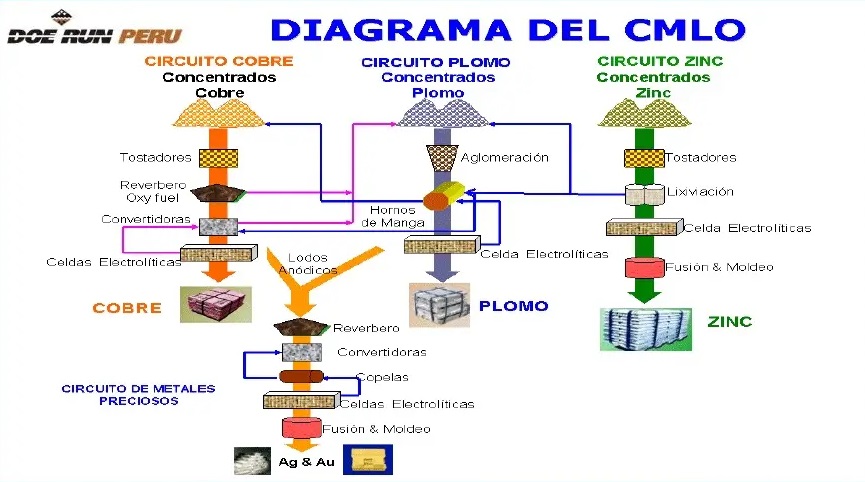
- Pirometalurgia
Durante el procesado pirometálico, un mineral, después de ser beneficiado, es decir, concentrado mediante machaqueo, trituración, flotación y secado, se sinteriza o tuesta (calcina) con otros materiales, tales como el polvo de la cámara de sacos filtrantes y fundente. A continuación, el concentrado se funde en un horno de cuba para obtener un lingote fundido impuro que contiene los metales deseados. Este lingote se somete seguidamente a un tercer proceso pirometálico para refinar el metal hasta conseguir el nivel de pureza deseado. Cada vez que se calienta el mineral o el lingote, se crean materiales residuales. El polvo procedente de la ventilación y los gases del proceso puede capturarse en una cámara de sacos y eliminarse o devolverse al proceso, dependiendo del contenido metálico residual. También se captura el azufre del gas, y cuando las concentraciones son superiores al 4 % puede convertirse en ácido sulfúrico. Dependiendo del origen del mineral y del contenido residual del metal, se puede obtener también como subproductos a diversos metales, por ejemplo, el oro y la plata (McCann, 2012).
Tipos de procesos pirometalúrgicos
- La tostación
La tostación es un importante proceso pirometalúrgico. La tostación por sulfatado se utiliza en la producción de cobalto y zinc. Su fin es separar los metales de forma que puedan transformarse en una forma hidrosoluble para el ulterior proceso hidrometalúrgico.

Tostación del Cobre. Fuente: https://web.facebook.com/ICI.Pagina.Oficial/photos/a.383083808475588/4561649677285626/
- La fusión
La fusión de los minerales sulfurosos produce un concentrado de metal parcialmente oxidado (mata). En la fusión, el material inservible, generalmente hierro, forma una escoria con el material fundente y se convierte en óxido. Los metales útiles adquieren la forma metálica en la etapa de conversión, que tiene lugar en los hornos de conversión. Este método se utiliza en la producción de cobre y níquel. Se produce hierro, ferrocromo, plomo, magnesio y compuestos de hierro por reducción del mineral con carbón vegetal y un fundente (caliza); el proceso de fusión se realiza generalmente en un horno eléctrico.
- La electrólisis
La electrólisis de sales fundidas, empleada en la producción de aluminio, constituye otro ejemplo de proceso pirometalúrgico. La alta temperatura necesaria para el tratamiento pirometalúrgico de los metales se consigue quemando combustibles fósiles o utilizando la reacción exotérmica del propio mineral (como, por ejemplo, en el proceso de fundición a la llama).
- La fundición a la llama
El proceso de fundición a la llama es un tipo de proceso pirometalúrgico ahorrador de energía en el que el hierro y el azufre del concentrado de mineral se oxidan. La reacción exotérmica, acoplada a un sistema de recuperación de calor, ahorra una gran cantidad de energía para la fusión. La elevada recuperación de azufre del proceso es también beneficiosa para la protección del medio ambiente. La mayoría de las fundiciones de cobre y níquel construidas recientemente utilizan dicho proceso.
Video 2: PROCESO DE FUNDICIÓN Y REFINACIÓN DE COBRE
-
Hidrometalurgia
Es una rama de la metalurgia que se centra en la extracción y recuperación de los elementos de interés a través de soluciones líquidas y acuosas, empleando la lixiviación (Alsimet, 2021). Permiten la extracción y obtención de metales y/o compuestos desde sus minerales o materiales de reciclaje (chatarras, escorias, cementos metálicos, barros anódicos, etc). Es decir, el metal puro se extrae a partir de reacciones químicas en la solución que lo contiene. Se opera con temperaturas bajas y presiones de hasta 5.000 kPa. Por norma general se someten a este proceso minerales que se han lixiviado con anterioridad. Se emplea en el oro, cobre y zinc, obteniéndose de esta forma soluciones concentradas de sulfatos de cobre.
La hidrometalurgia es un proceso más sencillo que la pirometalurgia, además de mucho menos contaminante. En la parte negativa se encuentra la alta acidez de trabajo y que, en algunos casos, se generan residuos tóxicos. Asimismo, es un proceso menos eficaz porque se usan temperaturas bajas, lo que afecta a las tasas de reacción química. Algunos ejemplos de procesos hidrometalúrgicos son la lixiviación, la precipitación, la reducción electrolítica, el intercambio iónico, la separación por membranas y la extracción con disolventes, sin embargo, se considera a tres ramas importantes (Alsimet, 2021).
Video 3: HIDROMETALURGIA DEL COBRE: MINA RADOMIRO
- Lixiviación
- Concentración y Purificación
- Precipitación
Tipos de procesos hidrometalúrgicos
Video 4: PROCESO GENERAL DE METALURGIA
1) Preparación de los minerales: Las principales operaciones de preparación de los minerales son:
- Trituración y molienda
Tienen por objeto reducir el tamaño de los minerales, siendo más pequeño el tamaño de las partículas obtenidas tras la operación de molienda. La trituración se realiza con materiales secos, mientras que la molienda puede hacerse con materiales secos o húmedos.
- Concentración
Tiene por objeto separar de un mineral la mayor parte de la ganga, de forma que el mineral quedará enriquecido o concentrado. La flotación es la operación más empleada para la concentración de las menas utilizadas en hidrometalurgia.
2) Extracción del metal. La extracción del metal por hidrometalurgia se realiza mediante las siguientes operaciones, una a continuación de la otra:
- Lixiviación
Operación en la que tiene lugar el ataque químico, en fase acuosa, del metal valioso contenido en la mena mineral. Puede ser ácida, básica o neutra dependiendo del carácter del reactivo químico utilizado, que a su vez es función de la ganga del mineral.
- Purificación y/o concentración
Operación que se realiza sobre la disolución obtenida en la etapa anterior de lixiviación. El objetivo de esta operación es retirar determinadas impurezas de la disolución antes de que ésta sea sometida a la etapa siguiente de precipitación. Se suele realizar mediante los siguientes métodos:
- Métodos químicos de precipitación.
- Cementación (reacción de desplazamiento similar a la metalotermia pero en fase acuosa).
- Utilizando cualquiera de las reacciones de la química convencional que sirven para retirar un metal de una fase acuosa.
- Extracción con disolventes (en el caso de disoluciones muy diluidas).
- Separación con resinas de intercambio iónico (en el caso de disoluciones muy diluidas). Precipitación: el objetivo de esta operación es separar el metal valioso de la disolución, en forma elemental (casi siempre) o en forma oxidada (en raras ocasiones). Se suele realizar mediante los siguientes métodos:
- Electrólisis (como es el caso del cobre).
- Cementación (como es el caso de las disoluciones cianuradas de oro).
- Métodos convencionales de química, como, por ejemplo, la precipitación de metales con hidrógeno gaseoso a presión y temperaturas altas (como es el caso del níquel y el cobre).
Usualmente, los procesos metalúrgicos son una combinación de procesos piro e hidrometalúrgicos, según el concentrado de mineral a tratar y el tipo de metal a refinar. Un ejemplo es la producción de níquel.
- Electrometalurgia
Esta rama emplea energía eléctrica para producir y tratar los metales. La convierte en calor para generar la temperatura adecuada para el proceso o bien para ayudar a descomponer un compuesto por acción electrolítica cuando el calor utilizado es bajo o bien por electrólisis cuando es mayor. Se puede aplicar en soluciones acuosas o en sales fundidas. En el primer caso se utiliza sobre todo para cobre, zinc, níquel, cobalto, plomo, plata, oro y otros metales como cadmio, cromo, manganeso, galio, titanio o telurio. En el segundo, para aluminio, litio, magnesio, sodio y potasio, así como para tierras raras (Alsimet, 2021).
Según el tipo de depósito que se obtiene, hay distintos procesos electrometalúrgicos: la electro obtención de metales, la electrorrefinación, la galvanoplastia o electrodeposición y el electroconformado. El electro obtención o precipitación por reducción electrolítica es uno de los procedimientos más sencillos para recuperar oro y plata, con un coste operacional ajustado cuantas menos impurezas tienen las soluciones. Además, permite refinar el cobre obteniendo cátodos de alta pureza. La electrorrefinación se emplea para el cobre, y la galvanoplastia sobre todo para oro, plata, platino y zinc. También es usada para evitar la corrosión de los metales, al crear una capa delgada protectora sobre el metal. Por su parte, con el electroconformado se elaboran moldes rápidos (Alsimet, 2021).
Video 5: ELECTROMETALURGIA
Tipos de procesos electrometalúrgicos
- Electro obtención de metales
Consiste en la extracción de metales a partir de soluciones, en forma de depósitos metálicos puros, densos y compactos o depósitos metálicos en polvo (pulvi-electrometalurgia) o bien, depósitos de compuestos metálicos (óxidos, hidróxidos o sales).
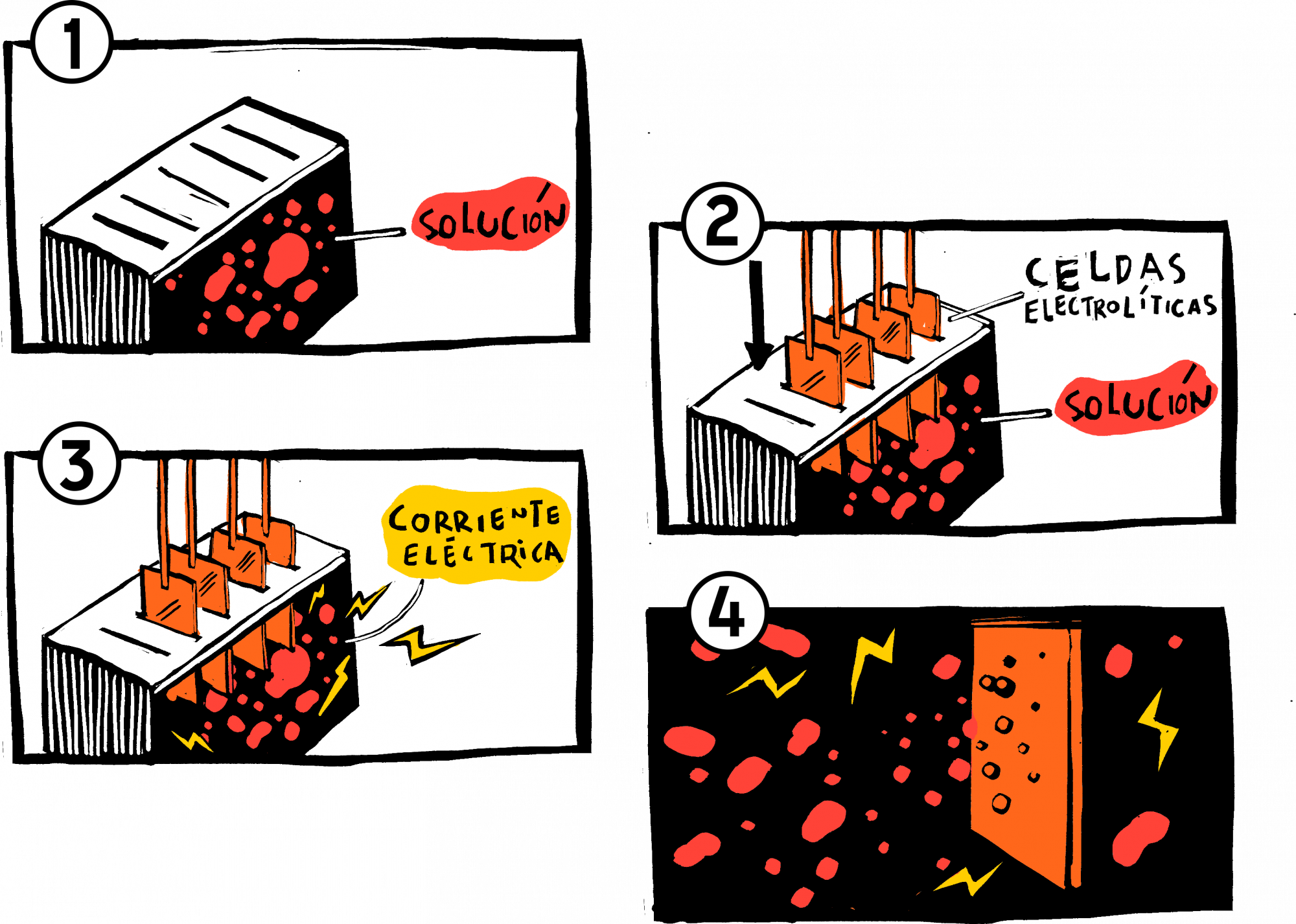
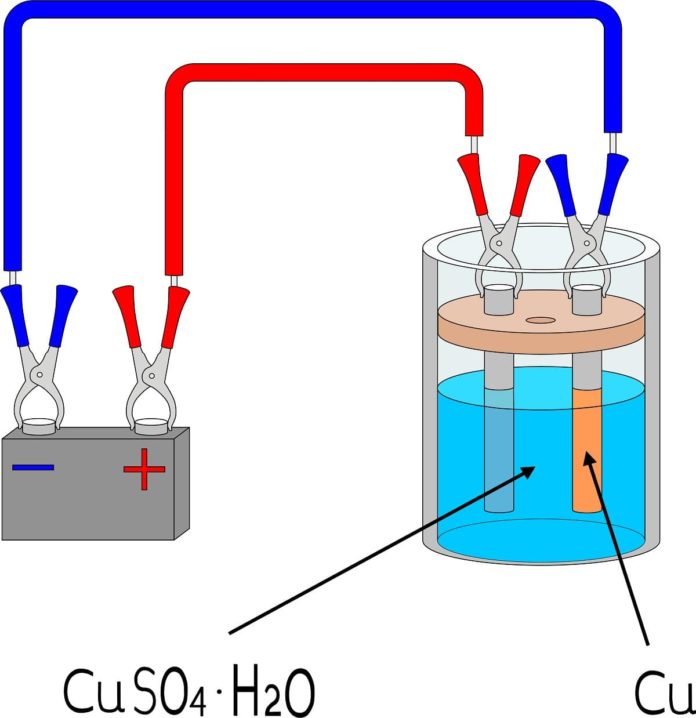
Proceso de electroobtención de cobre. Fuente: https://www.codelcoeduca.cl/codelcoeduca/site/edic/base/port/electroobtencion.html
- Electrorefinación de metales
Consiste en la obtención de depósitos metálicos de alta pureza a partir de un metal impuro.
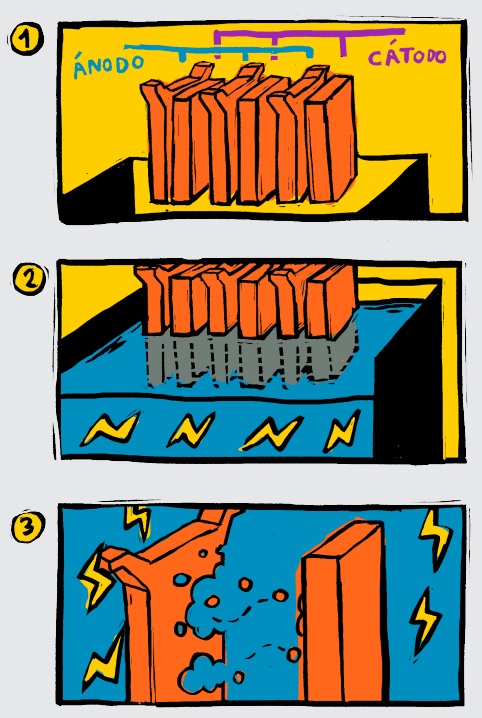
Electrorefinación. Fuente: https://www.codelcoeduca.cl/codelcoeduca/site/artic/20190109/asocfile/20190109005034/electrorefinacion_media_t__cnico_060119.pdf
- Galvanoplastia
Consiste en recubrimientos metálicos delgados con fines anticorrosivos o estéticos (cromados).
- Electroconformado
Consiste en la elaboración de piezas metálicas especiales por vía electrolítica.
Video 6: ELECTROFORMING
Impacto ambiental
Las emisiones de gases irritantes y corrosivos como el dióxido de azufre, ácido sulfhídrico y cloruro de hidrógeno, pueden contribuir a la contaminación del aire y originar fenómenos de corrosión de los metales y el hormigón, tanto en la planta como en el ambiente circundante. La tolerancia de la vegetación al dióxido de azufre depende del tipo de bosque y suelo. En general, los árboles con perennes toleran menores concentraciones de dióxido de azufre que los caducos (McCann, 2012).
Las emisiones de materia en partículas pueden contener elementos inespecíficos, fluoruros, plomo, arsénico, cadmio y muchos otros metales tóxicos e impurezas. Los residuos sólidos pueden estar contaminados con arsénico, plomo, sulfuros de hierro, sílice y otros contaminantes más. La gestión de la fundición debe comprender la evaluación y control de las emisiones procedentes de la planta, trabajo que solo debe realizar personal muy especializado con las propiedades químicas y toxicidades de los materiales emitidos en los procesos (McCann, 2012). En los procesos de flotación, tales como la concentración de cobre, se utilizan grandes cantidades de agua. La mayor parte de esta agua se recicla y se devuelve al proceso. Los residuos, o colas, del proceso de flotación se bombean en forma de lodos a estanques de sedimentación. El agua se recicla al proceso. El agua de proceso que contiene metal y el agua de lluvia se limpian en plantas de tratamiento antes de su vertido o reciclaje. Los residuos sólidos comprenden escorias de fundición, lodos de descarga producidos en la conversión de dióxido de azufre en ácido sulfúrico y lodos procedentes de balsas, por ejemplo, estanques de sedimentación. Algunas escorias pueden concentrarse y devolverse a las fundiciones para someterlas a un nuevo proceso o para la recuperación de otros metales presentes. Muchos de estos residuos sólidos son peligrosos y deben almacenarse de acuerdo con la normativa ambiental (McCann, 2012).
Existen pruebas de exposición a vapores metálicos de mercurio y metilación de mercurio en la naturaleza, especialmente en zonas donde se procesa el oro. En un estudio del agua, depósitos y peces de zonas mineras de Brasil donde se extrae oro, las concentraciones de mercurio en las partes comestibles del pescado que se consume localmente eran casi seis veces superiores al nivel recomendado oficialmente en ese país para el consumo humano (Palheta y Taylor 1995). En una zona contaminada de Venezuela, buscadores de oro han estado utilizando mercurio durante varios años para separar el oro de las arenas y el polvo de roca auríferos. El alto nivel de mercurio existente en las capas superficiales del suelo y en los sedimentos de goma de la zona contaminada constituye un grave riesgo para la salud de todas las personas alrededor. La contaminación por cianuro de las aguas residuales es también causa de gran preocupación, por ello, las disoluciones de cianuro deben tratarse antes de su evacuación, o bien recuperarse y reutilizarse (McCann, 2012).
El estado físico del material, la temperatura a la que abandona el proceso y la presencia de otros materiales, son todos factores que han de tenerse en cuenta al planificar las medidas de control de la contaminación aérea. También, es deseable contar con una estación meteorológica, que lleve los archivos meteorológicos y estar preparados para reducir la salida de emisiones cuando las condiciones climáticas no favorezcan la dispersión de los efluentes aéreos. Son necesarias investigaciones de campo para observar los efectos de la contaminación aérea sobre las áreas residenciales y agrícolas. El dióxido de azufre es uno de los principales contaminantes que se recupera en forma de ácido sulfúrico cuando su cantidad es suficiente. Comúnmente, para cumplir las normas sobre emisiones de gases tóxicos, las emisiones de partículas se controlan mediante filtros textiles y cubas de precipitación electrostáticas (McCann, 2012).
Video 7: DAÑOS AMBIENTALES DE LA MINERÍA EN EL PERÚ: ¿QUÉ HACER CON ELLOS?
Ventajas y desventajas de la explotación de la mina de litio descubierta en el Perú:
-
Ventajas:
- La mina de Flachani tiene la capacidad de convertirse en un productor de larga vida útil y bajo costo.
- Hoy las empresas no sólo deben buscar y actuar en su propio beneficio, sino que deben incluir otros aspectos a favor de la sociedad como los económicos, sociales y políticos.
- Es importante reconsiderar el ingreso económico familiar al momento de aceptar la explotación de la mina Falchani, la promoción del desarrollo económico, el bienestar social y las inversiones extranjeras.
- Promocionar y poner en práctica el desarrollo económico sostenible en las comunidades del distrito de Corani- Puno
- La inversión extranjera en minería puede ser el salvavidas en la economía peruana, el cual tuvo una crisis por la pandemia de coronavirus, sin embargo, la reactivación económica, establecido por el gobierno permitió retomar la exploración y explotación minera; las empresas mineras están tratando de recuperar sus inversiones y, en especial, el proyecto minero de Litio sigue avanzando en la etapa de exploración mediante la inversión extranjera, se espera que este proyecto minero ayude a la reactivación económica en la región de Puno.
- El gobierno local y regional, en materia ambiental debe ir avanzado en los aspectos de mitigación ambiental, aplicando leyes relacionado a la conservación y preservación del medio ambiente en las actividades de exploración y explotación de minerales; pues, los problemas sociales y ambientales derivados de la actividad minera, son de plena responsabilidad del Estado y, por ende, del gobierno municipal del distrito de Corani
-
Desventajas:
-
- El sector minero es el que más ha contribuido en la contaminación del medio ambiente (ríos, lagunas, tierras de cultivo, aire, entre otros), lo cual se evidencia notablemente los efectos negativos en el Lago Titicaca; por lo que, se espera que los efectos contaminantes en este sector sigan en aumento al explotar la mina de Litio, junto con el crecimiento de la economía, por ende, es uno de los sectores que más acciones de mitigación demanda
- “Los impactos de la actividad, en especial sobre el recurso agua, hacen que estos proyectos sean percibidos por un porcentaje mayoritario de la población como una amenaza al medio ambiente y a la salud” (Bastidas et al., 2019, p. 203).
- “El exceso de contaminantes en el medio ambiente, pueden provocar efectos irreversibles y serios a la salud, en especial a las féminas” (Estrada et al., 2016, p. 86).
- Una vez disgregado el mineral, el siguiente paso consiste en extraer el elemento que tiene importancia económica (uranio, plata, litio), la separación de los materiales inertes se logra mediante productos químicos, como es el caso del ácido sulfúrico, lixiviación con cianuro; también por tratamiento superficial en los materiales sulfurados, con los tiofosfatos orgánicos, tiocarbamatos y tioureas. El proceso no termina ahí, pues hay que agregar espumantes y otros productos químicos para que pueda flotar la parte útil y desechar la materia estéril o relave.
- La actividad minera extrae, transporta y disgrega grandes volúmenes de rocas, en los cuales emplean muchos productos químicos como el nitrato de amonio (explosivos), supresores de polvo, entre otros.
- La degradación del medio ambiente por un contaminante externo puede provocar daños en la vida cotidiana del ser humano y alterar las condiciones de supervivencia de la flora y la fauna.
- Las actividades mineras y el proceso de modernización, traen como consecuencias la pérdida de identidad comunitaria, el abandono de la agricultura, procesos de cambio de uso del suelo y cambios en la dieta alimentaria, entre otros
- Los impactos negativos en el medio ambiente, son una amenaza para las futuras generaciones, debido a la reducción de áreas forestales, la pérdida de la biodiversidad, los eventos hidrometeorológicos más frecuentes e intensos, la pérdida de la agroproductividad, la reducción de las áreas de cultivo, la afectación de los manglares y los ecosistemas costeros, así como el incremento de la vulnerabilidad de los asentamientos costeros.
Video 8: ¿QUÉ ES EL LITIO? TE CONTAMOS TODO LO QUE ES Y SUS USOS
Entonces, sabiendo que la minería trae beneficios, pero también perjuicios como equipo tomamos una postura al respecto respondiendo estas preguntas:
¿Qué debería hacerse con estas reservas de litio? ¿Debe extraerse litio de esta mina?
La respuesta corta es sí. Ahora explicaremos la importancia de este metal en el mundo y la razón por la que puede ser más beneficioso de lo que parece.
El cambio climático es real y este se produce, en mayor medida, por las emisiones de gases de efecto invernadero. De acuerdo a la ONU, más del 60% de estos gases lo producen la quema de combustibles fósiles. Estas actividades no se pueden dejar de hacer debido a que proporcionan gran parte de la energía global. Por esto, es recomendable el uso de las energías limpias, las cuales son renovables y no emiten estos gases (ONU).
Las energías renovables no permiten una generación continua; por ejemplo, la energía solar, la cual solo puede adquirirse cuando es un día soleado. Debido a esto surge la necesidad de almacenar la energía en baterías. También, con la finalidad de dejar de consumir combustibles fósiles para el uso de automóviles, se crearon los autos eléctricos. Estos requieren de baterías para almacenar la energía eléctrica (Manrique, 2014, p.4).
La necesidad de baterías para el mundo moderno crece y, por lo tanto, su demanda también. En ese contexto entra el litio como el metal del que se pueden crear las mejores baterías. Las propiedades de este metal hacen posible que las baterías sean muy efectivas: tienen buena durabilidad, carga rápida y espacio más compacto que otras baterías.
El litio es un metal raro, ya que normalmente se encuentra en extensos salares y forman parte de minerales de baja concentración. Debido a su rareza y a la importancia que adquirió, el precio del litio ha aumentado. Según comenta un informe del Centro de Estudios Estratégicos e Internacionales, el precio del litio se duplicó entre 2016 y 2018 y se vaticina que se multiplicará por ocho de aquí a 2027 (CENE, 2021).
Entonces, concluimos como equipo que sí debería ser explotado la mina Falchani, no solo debemos verlo como una potencial fuente de ingresos para el país y para la región Puno; sino que también debemos pensar que la extracción de ese mineral contribuirá al uso de energías renovables a nivel local y mundial. Asimismo, contribuirá con modernizar el departamento, generar un crecimiento tanto económicamente, con la educación, salud y visionariamente para las personas locales. Por ende, consideramos que presenta más beneficios que desventajas si bien es cierto la contaminación ambiental que se generaría será exponencial sin embargo a largo plazo se trataría de remediar ello implementando y descubriendo nuevas tecnologías eco amigables que requieran litio en su fabricación para ser usadas.
Bibliografía:
- Almacenes Sidero-Metalurgico S.A. (2021). Procesos metalúrgicos industriales: Pirometalurgia, Hidrometalurgia y Electrometalurgia.http://alsimet.es/es/noticias/procesos-metalurgicos-industriales-pirometalurgia-hidrometalurgia-y-electrometalurgia
- Arista, A., Ayala, A., Crispin, F., y Lopez, J. (2019, 15 junio). METALES Y MINERALES. Blog del curso de Química 2 Prof. P. Morales B. http://blog.pucp.edu.pe/blog/qm2-202-131/2019/11/16/metales-y-minerales-3/
- Centro de Estudios de la Nueva Economía de la Universidad de Belgrano (CENE). (2021) Litio: La nueva esperanza argentina (Boletín informativo N° 206-2021). http://repositorio.ub.edu.ar/handle/123456789/9233
- International Council of Mining & Metal. (s.f.). La minería y los metales. https://www.icmm.com/es/mineria-y-los-metales
- Junta de Castilla y León. (2008). Los Metales en Castilla y León. La Sociedad de Investigación y Explotación Minera de Castilla y León, S.A.https://www.siemcalsa.com/images/pdf/Los%20metales.pdf
- Manrique, A. (2014). Explotación del litio, producción y comercialización de litio en Argentina. [Trabajo final integrador de postgrado, Universidad Nacional de Mar del Plata] http://rinfi.fi.mdp.edu.ar/xmlui/handle/123456789/63
- McCann, M. (2012). Capítulo 82 Metalurgia y metalisteria. Instituto Nacional de Seguridad e Higiene en el Trabajo.https://www.insst.es/documents/94886/161971/Cap%C3%ADtulo+82.+Metalurg%C3%ADa+y+metalisteria
- Muñoz, M. (2016). Extracción de metales por hidrometalurgia: Procesamiento de cobre y cinc. Universidad Politécnica de Valencia.https://riunet.upv.es/bitstream/handle/10251/68321/Mu%C3%B1oz%20-%20Extracci%C3%B3n%20de%20metales%20por%20hidrometalurgia%3A%20Procesamiento%20de%20cobre%20y%20cinc.pdf?sequence=1
- Nickel, E. (1995). Definición de Mineral. (Boletín de la sociedad Española de Mineralogía). Comisión de Nomenclatura Mineral y Minerales Nuevos de la Asociación Mineralógica Internacional.https://es.scribd.com/document/469223177/Definicion-de-mineral-Nickel
- Ondarse, D. (2021). Metales. Argentina. de.https://concepto.de/metales/#ixzz7VIlU4Gng
- Organización de las Naciones Unidas. (s.f). Las ciudades y la contaminación contribuyen al cambio climático. https://www.un.org/es/climate-change/climate-solutions/cities-pollution
- Simpson, J. (2003). Hidrometalurgia. Bernd, E . Introducción a la metalurgia. (pp.188-201). Universidad de Santiago de Chile Facultad de Ingeniería.https://metalurgia.usach.cl/sites/metalurgia/files/documentos/capitulo14.pdf
- Toledo, P. (2020, 16 noviembre). ¿Qué son los minerales en la Geología?. Revista Ciencias de la Tierra.https://revistacienciasdelatierra.com/geociencias/mineralogia/que-son-los-minerales-en-la-geologia/5312/
- Yanque, S., Huaman, F., Ramirez, E., Chua, M. y Brocos, S. (2019, 15 junio). METALES Y MINERALES. Blog del curso de Química 2 Prof. P. Morales B. http://blog.pucp.edu.pe/blog/qm2-202-131/2019/06/15/metales-y-minerales-2/