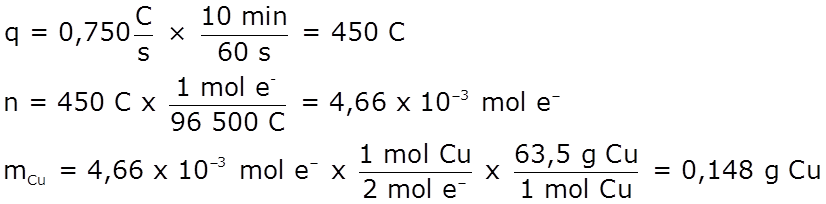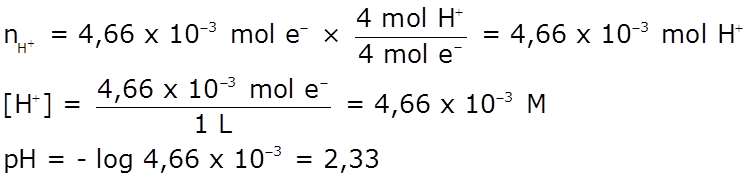4.3.4. Aspecto cuantitativo de la electrólisis
Aspecto cuantitativo
Según Faraday, la masa de un sustancia química, producto de la electrólisis, es directamente proporcional a la corriente que pasa a través de la celda.
En consecuencia, la cantidad de carga aplicada se determina por:
q = I x t
donde:
q = carga
I = intensidad de corriente
t = tiempo
Además:
- 1 Coulombio = 1 Ampere x segundo
- 1 mol de electrones transporta 96 500 Coulombios
- 1 F = 96 500 C = 1 mol de e-
En consecuencia, podemos calcular el número de moles de electrones transportados por la cantidad de corriente suminstrada durante el tiempo de paso de la corriente aplicada.
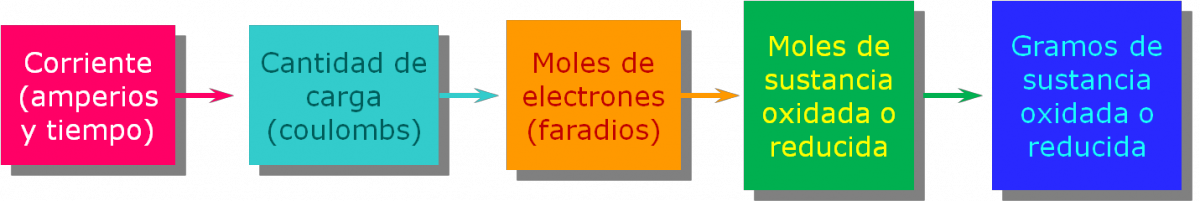
A continuación se muestra la relación entre las cantidades de sustancias producidas o consumidas en la electrólisis y la cantidad de carga eléctrica que se utiliza. Son las mismas relaciones aplicables a las celdas galvánicas.
 |
Recuerda
- Es importante contar con el balance correcto de las medias reacciones que transcurren en los electrodos, ánodo y cátodo.
- Ello nos permite relacionar el paso de la energía eléctrica a través de los electrodos, con las sustancias consumidas o producidas en los mismos.
- Es importante también, que comprendas que el número de moles de electrones o faradios que pasan por el ánodo y el cátodo, es el mismo para ambos electrodos.
|
 |
Problema
Para la electrólisis de CuSO4:
- Escribe las reacciones que se llevan a cabo en cada uno de los electrodos;
- Determina qué masa de cobre se deposita sobre el cátodo ante el paso de 0,750 A, que fluyen durante 10 minutos
- Si el volumen de la solución es de 1 L, determina cuál será el pH al final del proceso.
Solución:
♦ Ánodo: oxidación del agua:
2 H2O(l) → O2(g) + 4 H+(ac) + 4 e–
Cátodo: reducción del Cu2+:
Cu2+(ac) + 2 e– → Cu(s)
| ♦ |
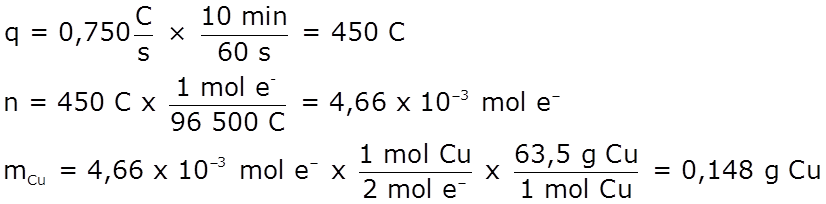 |
| ♦ |
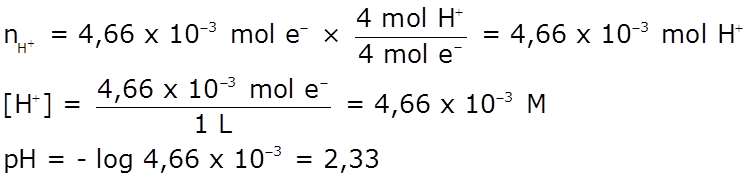 |
|