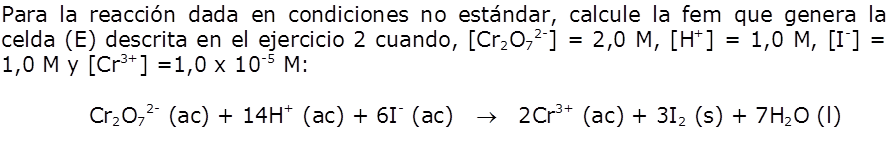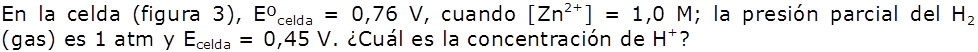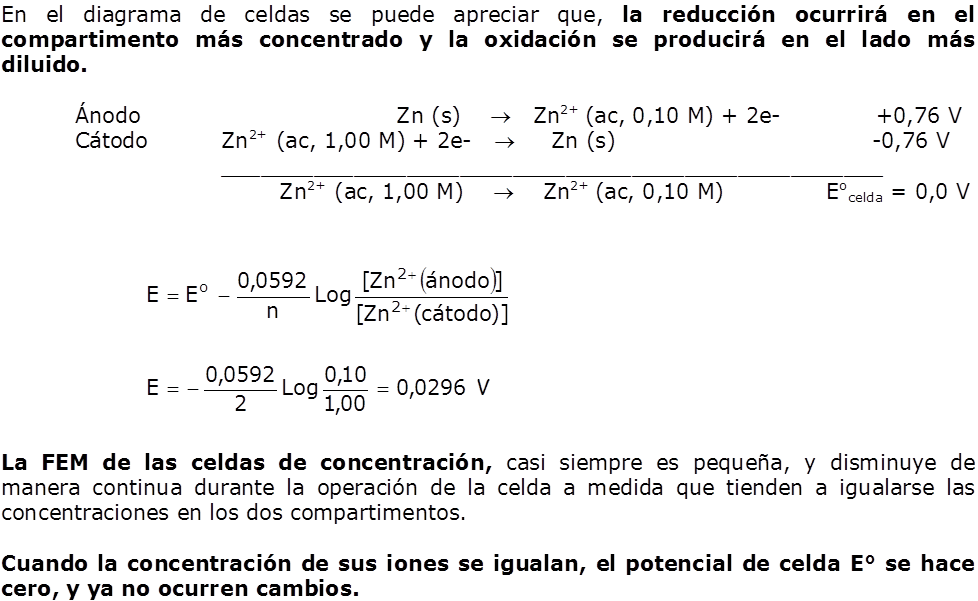4.2.3.1 Efecto de la Concentración sobre al FEM de la celda. Ecuación de Nernst
Hasta el momento, hemos podido calcular el E0(Celda), haciendo uso de los Potenciales Estándar de Reducción a 25°C, lo que quiere decir que hemos encontrado el Potencial de Celda, pero a condiciones estándar.
Los estudios realizados sobre celdas galvánicas, han revelado que hay una depedncia entre la concentrarción de reactivos y productos en la reacción de la celda y la FEM.
Cuando la concentración de los reactivos aumenta, la FEM también lo hace; cuando la concentración de los productos aumenta la FEM disminuye.
La mayoría de la reacciones, no se producen a condiciones estándar, ¿cómo encontrar la FEM para celdas que no se encuentran a condiciones estándar?
La Ecuación de Nernst, nos permite calcular la FEM, que se genera en condiciones diferentes al estándar.
Nernst, durante el desarrollo de su investigación, para encontrar la FEM a condiciones diferentes del estándar, La ecuación de Nernst, se obtiene a partir de la dependencia que existe entre la FEM de la celda y el cambio de energía libre ΔG en condiciones diferentes al estándar.
La ecuación de Nernst se obtiene, a partir de la :
La ecuación de Nernst, nos permite encontrar la FEM que produce la celda en condiciones no estándar, o encontrar la concentración de un reactivo o producto midiendo la FEM de la celda.Problema
 |
Problema |
| Solución | 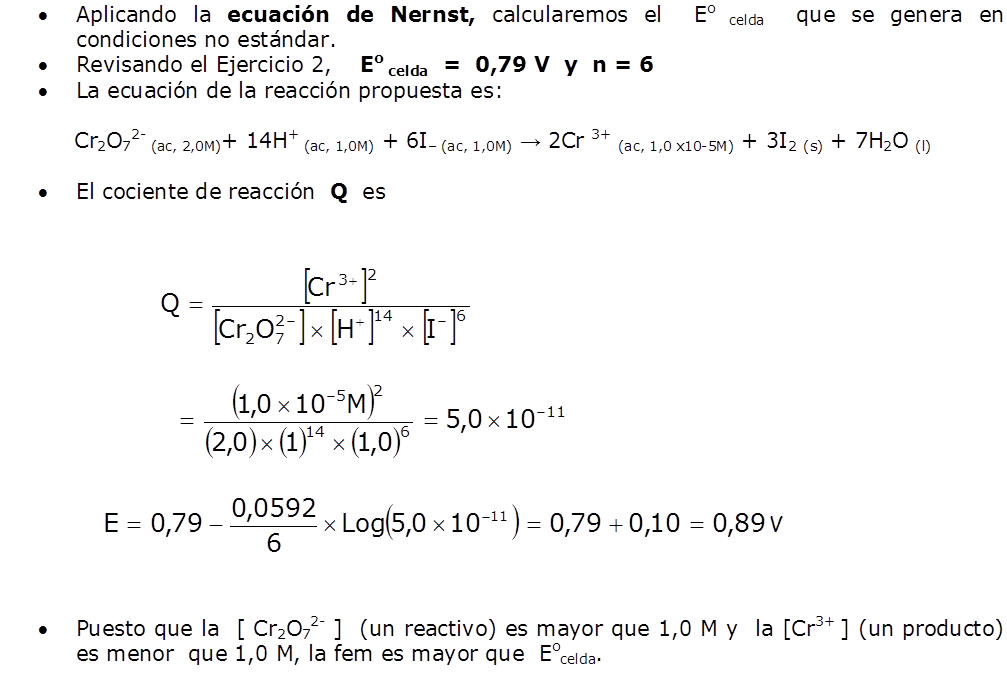
|
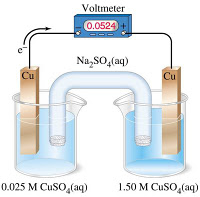
Celdas de Concentración
Si analizamos la figura anterior, podemos observar que tanto el recipiente anódico como el catódico, tiene la misma solución, solo que a condiones diferentes; y que los dos electrodos son del mismo material. Pero sin embargo vemos que hay un potencial de celda registrado.
¿Cómo se explica esto?
Hemos establecido que el potencial de los electrodos, depende de las concentraciones, es posible construir una celda con dos semiceldas hechas del mismo material pero con diferente concentración iónica. A este tipo de celda se le conoce como celda de concentración.
Analicemos la siguiente celda:
Zn (s) / Zn2+ (ac, 0,10 M) // Zn2+ (ac, 1,00 M) / Zn (s)