1.2 Estados de la materia
Unidad 1: Introducción al estudio de la materia
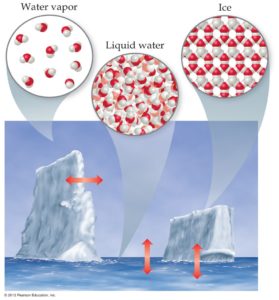
Más de una vez habrás observado lo que ocurre mientras hierve un poco de agua, cómo se forman unas burbujas en su interior, las que luego ascienden a la superficie y se desprende vapor que se disemina en el ambiente. Por otro lado, qué ocurre cuando colocas unos cubos de hielo en tu vaso con refresco y lo dejas un momento, el tamaño de éstos va disminuyendo hasta que desaparecen, ¿verdad?; los cambios que has observado en estos dos procesos son simplemente la manifestación de los tres estados en los que se presenta la materia.
En principio, todas las sustancias pueden existir en los tres estados de agregación en que se presenta la materia, sólido, líquido o gaseoso. La mayoría de sustancias se presentan en un estado concreto, por ejemplo los metales o las sustancias que constituyen los minerales se encuentran en estado sólido, el alcohol o el aceite en estado líquido y el oxígeno ,O2, o el dióxido de carbono, CO2, en estado gaseoso.
|
El estado sólido se caracteriza por tener masa, volumen y forma definidos. Siempre que no apliquemos fuerzas que lo puedan deformar (como ocurriría con sustancias como la plastilina) o romper, la forma de un objeto sólido permanece fija, es decir no se pueden comprimir o expandir. |
El estado líquido se caracteriza por tener masa y volumen fijos, pero forma variable. Las sustancias líquidas adoptan la forma del recipiente que las contiene. Tampoco es posible comprimir o incrementar su volumen. |
El estado gaseoso se caracteriza por tener masa fija, pero forma y volumen variables. Los gases adoptan la forma y ocupan todo el volumen del recipiente que los contiene. |
Las condiciones que presenta nuestra superficie terrestre, permite que sólo algunas sustancias puedan hallarse de forma natural, en los tres estados, como en el caso del agua.
|
Tomado de Brown T. et al. Química: la ciencia central, 2014 |
Existe un cuarto estado de agregación, el plasma, que no está presente en cualquier parte, pero la encontramos por ejemplo en bulbos de luz fluorescente o las luces de neón. El plasma se halla también en el sol y las estrellas, que son grandes bolas de gases a temperaturas realmente altas. Los plasmas son bastante parecidos a los gases, pero los átomos son diferentes porque están ionizados los iones generándose electrones libres que han sido arrancados de sus átomos por efecto del calor o la electricidad.