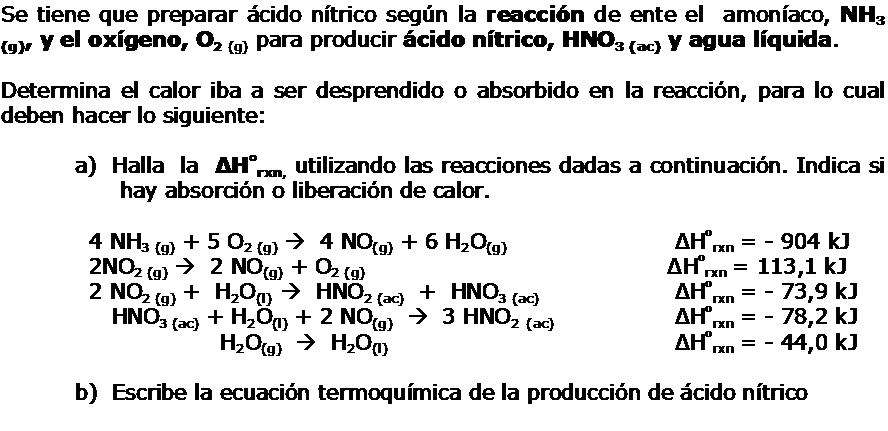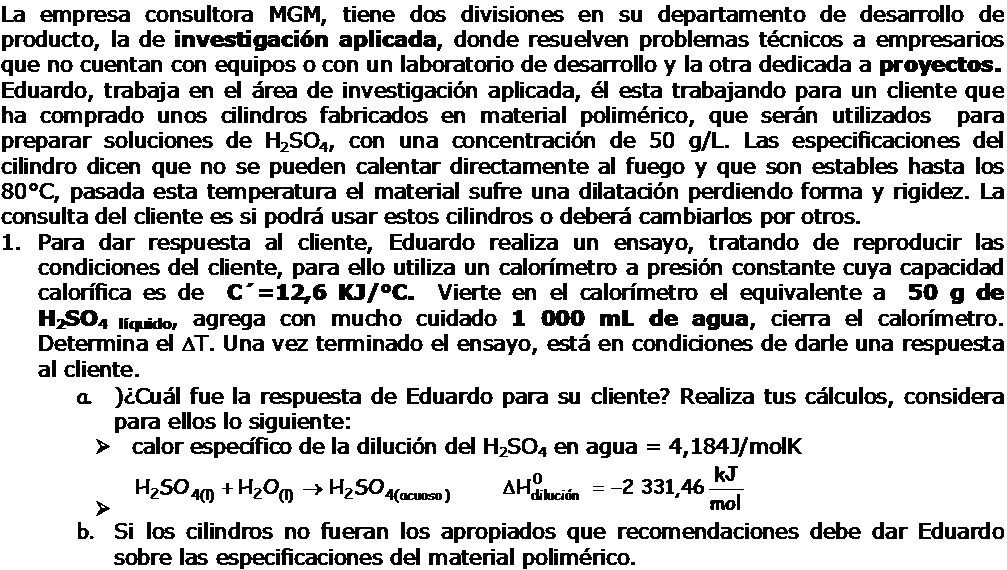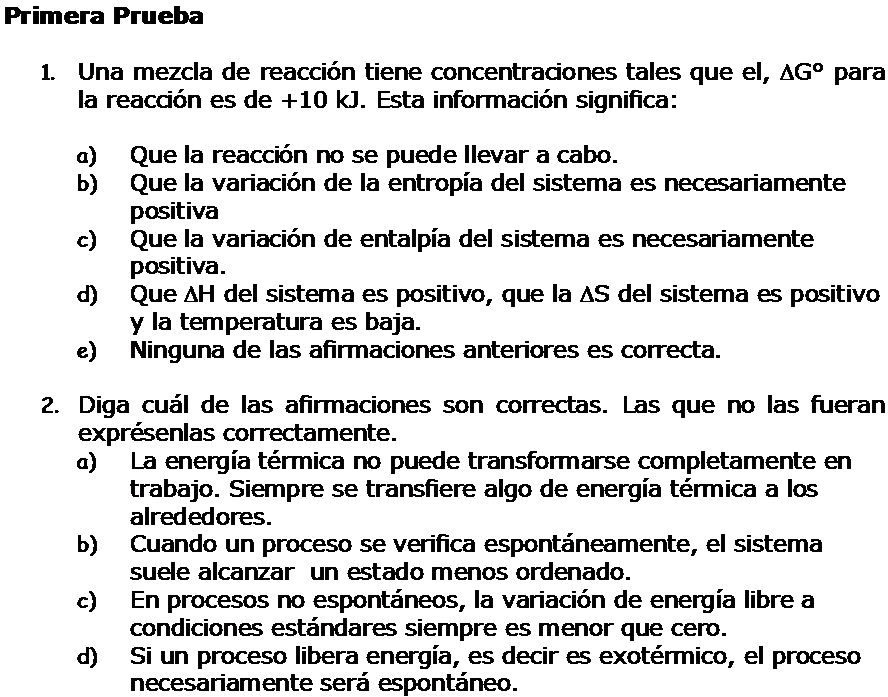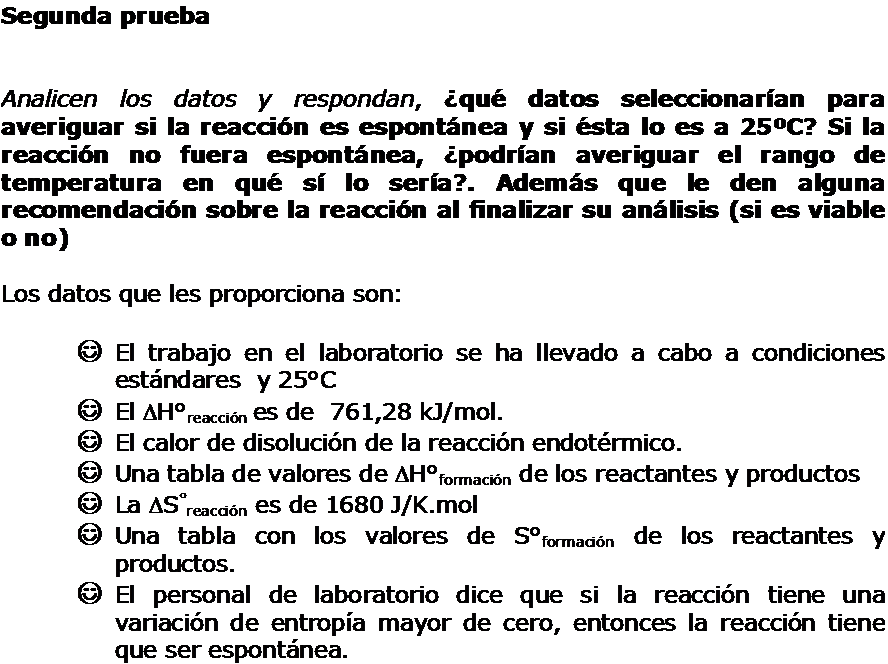1.8.-Conclusiones de la Termodinámica
Siempre que se plantee una reacción química es necesario conocer:
- El calor de reacción, conocer si la reacción es exotérmica o endotérmica. Esto permitirá saber cuanta energía debemos suministrar o cuanta energía liberará la reacción en cuestión.
- Si la reacción será espontanea o no. Se puede calcular con:
- valores de Variación de la Entropía del Universo. Si el valor es positivo sucederá espontánemente la reacción; pero si es negativo nos indicará que la reacción no courre espontáneamente.
- valores de la Energía libre de Gibbs. Si el valor es negativo la reacción es espontánea; si el valor es positivo señalará que la reacción no ocurre de manera espontanea.
- podemos tambien calcular a que condición se volverá espontánea la reacción, analizando si debemos aumentar o disminuir la temepratura de reacción, o modificar las concentraciones de los reactantes y productos.