Autores:
- Bellatin A., Luciano
- Meza Y., Raúl
- Salazar C., Franz
Introducción
La demanda por tecnologías verdes apremia debido a las preocupaciones ambientales. Los líquidos iónicos, llamados disolventes verdes, pueden utilizarse para una variedad de aplicaciones debido a sus propiedades físicas y químicas únicas, como su muy baja presión de vapor, su capacidad de reciclaje y bajo impacto sobre el medio ambiente. Sin embargo surge la pregunta: ¿es sostenible?; esto es, ¿el “verdor” de su producción supera o es equiparable al de sus aplicaciones?
Síntesis del tema
Líquidos iónicos y sus aplicaciones
Los líquidos iónicos son sales con puntos de fusión por debajo de los 100 °C, constituidos típicamente por cationes orgánicos grandes y asimétricos, asociados a aniones orgánicos e inorgánicos. Dentro de sus inusuales propiedades fisicoquímicas están la presión de vapor despreciable, alta estabilidad química y térmica, alto grado de solvatación para sustancias orgánicas, inorgánicas y poliméricas. Esto es aumentado por la variación de propiedades de acuerdo con la selección cuidadosa de iones. Dentro de sus aplicaciones más diversas están: solventes, medios de reacción, electrolitos, aditivos, síntesis orgánica, catálisis, procesos de extracción, electroquímica, nanotecnología, etc. (Dharaskar 2012; Chiappe et al. 2016).
Algunas aplicaciones adicionales y más específicas son: desulfuración de combustible líquido, ya que la aplicación de condiciones de proceso muy suaves (baja presión y temperatura) es una ventaja adicional de este nuevo enfoque en comparación con hidrodesulfuración tradicional. También pueden emplearse para la purificación de aceites esenciales mediante extracción, separación de mezclas azeotrópicas, en la purificación de hidrógeno, en la extracción de metales de tierras raras, en la extracción de los ácidos carboxílicos, para la eliminación de azufre de corrientes de refinería, en la separación de isómeros, etc. (Dharaskar. 2012).
Síntesis de líquidos iónicos
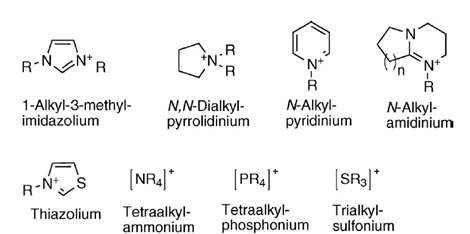
Se puede considerar que el primer líquido iónico preparado fue el nitrato de etilamonio en 1914. Es una neutralización ácido base entre ácido nítrico concentrado y etilamina, aunque tiene la gran desventaja de sufrir degradación a través de la desprotonación, por lo que su aplicación fue bastante limitada. De mayor aplicación son los siguientes cationes (McIntosh, 2016).
Figura 1: cationes encontrados en la mayoría de los líquidos iónicos. Imagen de McIntosh 2016.
Los métodos de obtención más comunes incluyen la alquilación del 1-metilimidazol. Tienen la ventaja de usar temperaturas moderadas, además del bajo costo del haloalcano empleado. Los flouroalcanos son muy poco reactivos, mientras que los yodoalcanos son tan reactivos que pueden ocurrir productos secundarios, además de la fotosensibilidad del yodo. Debido a esto se emplean los alcanos clorados o bromados en la reacción de adición. La alquilación también se puede producir sobre otras aminas como amidinas, trialquilaminas, pirrolidinas, piridinas, etc. El solvente en que se suelen realizar estas reacciones es acetato de etilo o tolueno (inmiscibles con el producto). Las impurezas que pueden presentarse son: compuestos orgánicos volátiles, impurezas de haluros por incompleta reacción, y otras impurezas iónicas. Se debería procurar eliminar las impurezas completamente con carbón activado o recristalización en acetonitrilo.
La síntesis puede ser asistida por microondas, alternativamente: se evita el uso del solvente, aunque si no es bien controlada, se produce la descomposición y la carbonización de los productos, resultando en productos secundarios. Esto es superable con calentamiento y agitación alternados (McIntosh, 2016).
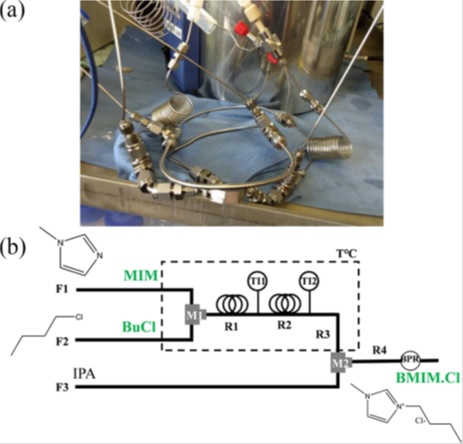
Más recientemente, Nakahara et al. (2019) desarrollaron un proceso de síntesis para el cloruro de 1-butil-3-metilimidazolio mediante un microrreactor de flujo continuo; primero mediante el análisis de la velocidad de reacción; luego, mediante una simulación, fue diseñado con una mejor eficiencia (para evitar el ensayo y error). Según su modelo, la producción podría ser mejorada hasta en casi 40 veces.
Figura 2: (a) Fotografía del microrreactor de flujo continuo. (b) Diagrama de flujo. Imagen de Nakahara et al. 2019.
Notable también es el trabajo desarrollado por Chiappe et al. (2016), en el que, para la síntesis del cloruro de 1-butil-3-metilimidazolio, el producto sirve también como el solvente de la reacción. Esto asegura una elevada velocidad de reacción, junto con alto grado de pureza.
Limitaciones de los líquidos iónicos
Algunos líquidos iónicos contienen aniones con halógenos, como:
AlCl4–, PF6–, BF4–, CF3SO3–, (CF3SO2)2N–
Que de alguna limitan su carácter verde. La presencia de átomos de halógeno puede causar problemas graves si la estabilidad a la hidrólisis del anión es pobre (por ejemplo, para [AlCl4]– y [PF6]–) o si se desea un tratamiento térmico de los líquidos iónicos usados (Dharaskar, 2012). En ambos casos se requiere un esfuerzo adicional para evitar la liberación de HF tóxico y corrosivo o HCl en el ambiente. Teniendo estos aspectos en mente, debe ser buscadas nuevas opciones de líquidos iónicos ‘más verdes’ para aplicaciones catalíticas industriales, que debe cumplir las siguientes propiedades deseadas:
- Punto de fusión o punto vítreo por debajo de 40 °C.
- Hidrólisis estable en solución acuosa neutra hasta 80 °C.
- Temperatura de descomposición térmica por encima de 250 °C.
- Posible eliminación por combustión sin formación de HF o HCl.
- Posible biodegradación del anión usado en el tratamiento de aguas residuales ordinaria.
- Síntesis a partir de materias primas baratas, técnicamente disponibles, por ejemplo, sales de metales alcalinos.
Sin embargo, muchos sistemas no cumplen con todo lo anterior dada la compleja combinación de propiedades. La disponibilidad técnica y la toxicología bien documentada de los líquidos iónicos son esenciales para su aplicación industrial.
Los líquidos iónicos que contienen cloruro como anión son una buena alternativa como agente de desulfuración (tratamiento de residuos de la industria del petróleo): poseen elevada capacidad para eliminar los compuestos de azufre, son estables al aire, la temperatura y la humedad; y los halógenos libres pueden ser fácilmente regenerados y reciclados.
Conclusiones
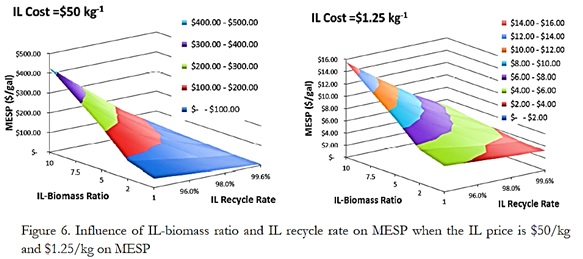
Luego de mencionar síntesis de líquidos iónicos y sus aplicaciones, podemos preguntarnos lo siguiente: ¿Cuál es el costo-beneficio de utilizar LI?, si bien el beneficio va por el lado de la sostenibilidad en los procesos químicos, hay algunos casos como en la biorefinería celulósica donde utilizar LI aumenta los rendimientos de extracción de carbohidratos; sin embargo, sintetizar LI como 1-ethyl-3-methylimidazolium acetate [C2C1im][OAc] es muy caro, lo que convierte en poco rentable su uso a grandes escalas; por esta razón en el 2014 en el Joint BioEnergy Institute, California, sintetizaron LI más económicos utilizando aminas alifáticas simples y de bajo costo (George, 2014).
Utilizar algunos LI como solventes de extracción puede resultar costoso por sus materias primas de síntesis; sin embargo, esta aseveración viene ligada al valor agregado del producto que se quiere extraer, de manera que si el producto genera grandes utilidades, promover su mayor producción, si bien costosa, será beneficiosa tanto económica como ambientalmente.
A medida que continúan las investigaciones y se desarrollan procesos más eficientes, el costo económico y medioambiental en la producción de líquidos iónicos irá disminuyendo, mientras sus aplicaciones irán en aumento.
Bibliografía
- GEORGE, A. BRANDT, S. M. S. NIZAN, D. KLEIN-MARCUSCHAMER, R. PARTHASARATHI, N. SUN, N. SATHITSUKSANOH, J. SHI, V. STAVILA, K. TRAN, S. SINGH, B. HOLMES, T. WELTON, B.A. SIMMONS, J.P. HALLETT,
2014 “Design of low-cost ionic liquids for ligoncellulosic biomass pretreatment”. UK: Royal Society of Chemistry. Green Chemistry. Vol. 17. Págs. 1728-1734.
CHIAPPE, Cinzia; MEZZETTA, Andrea; POMELLI, Christian S.; PUCCINI, Monica; SEGGIANI, Maurizia
2016 “Product as Reaction Solvent: An Unconventional Approach for Ionic Liquid Synthesis”. Italy. Organic Process Research & Development. Vol. 20. Págs. 2080-2084.
MATEO, F.; DE LOS RÍOS, A. P.; HERNÁNDEZ, F. J.; LOZANO, L. J.; GINESTA, A.; SÁNCHEZ, S.; GODÍNEZ, C.
2008+ “Uso de líquidos iónicos basados en cationes imidazolio y amonio como disolventes verdes para la recuperación selectiva de Zn (II), Cd (II), Cu (II) y Fe (III) de soluciones acuosas hidrocloradas” Cartagena C (Murcia).
MCINTOSH, Alastair; GRIFFITH, Jeraime; GRÄSVIK, John
2016 “Methods of Synthesis and Purification of Ionic Liquids. Application, Purification and Recovery of Ionic Liquids”. Págs. 59-99.
DOI: 10.1016/B978-0-444-63713-0.00002-X
NAKAHARA, Yuichi; METTEN, Bert; TONOMURA, Osamu; NAGAKI, Aiichiro; HASEBE, Shinji; YOSHIDA, Jun-ichi
2019 “Modeling and Design of a Flow-Microreactor-Based Process for Synthesizing Ionic Liquids”. Organic Process Research & Development. Vol. 23. Págs. 641-647.
PASSOS Helena, FREIRE Mara G. y COUTINHO João
2014 “Ionic liquids solutions as extractive solvents of value-added compounds from biomass”. UK: Royal Society of Chemistry. Green Chemistry. Vol. 16. Págs. 4786-4815.
SWAPNIL, Dharaskar
2012 “Ionic Liquids (A Review): The Green Solvents for Petroleum and Hydrocarbon Industries” Research Journal of Chemical Sciences. Nagpur, India. Vol. 2, N° 8. Págs: 80-85.